Ajuste la ecuación química y calcule la masa (en g) de Fe metálico que reaccionó.
QuímicaComunidad ValencianaPAU 2022Extraordinaria
Química · Comunidad Valenciana 2022
10 ejercicios90 min de duración
Ejercicio 1 · Bloque I
1Bloque I
2 puntosBloque IProblemas
El hierro metálico se disuelve en disoluciones de ácido clorhídrico, de acuerdo con la siguiente ecuación química (no ajustada):
Una pieza de Fe puro se disolvió en de una disolución de . Tras la reacción se determinó que la concentración de había disminuido hasta .
Calcule la concentración molar de en la disolución final.
Calcule el volumen (en litros) de dihidrógeno generado, medido a y .
Ejercicio 1 · Bloque II
1Bloque II
2 puntosBloque IICuestiones
Responda razonadamente a las cuestiones siguientes:
¿Qué átomo tiene mayor la primera energía de ionización, el calcio () o el germanio ()?
¿Qué átomo tiene mayor electronegatividad, el potasio () o el arsénico ()?
¿Qué átomo tiene mayor radio, el magnesio () o el cloro ()?
Ejercicio 2 · Bloque I
2Bloque I
2 puntosBloque IProblemas
En un reactor de 1 litro de capacidad, se introducen de y se calienta a . A esa temperatura se produce la disociación del , según la ecuación química:
Una vez alcanzado el equilibrio, el porcentaje de disociación del es del . Calcule:
La presión total en el interior del reactor una vez alcanzado el equilibrio.
El valor de las constantes y a la temperatura de trabajo.
Indique razonadamente si, al disminuir el volumen del reactor a la mitad, manteniendo la temperatura constante, el porcentaje de disociación del aumentará o disminuirá.
Ejercicio 2 · Bloque II
2Bloque II
2 puntosBloque IICuestiones
Responda a las siguientes cuestiones sobre estructura molecular:
Dibuje la estructura electrónica de Lewis de la molécula de diclorodifluorometano o freón–12 () y del metanal o formaldehído ().
Indique la hibridación del átomo de C en cada una de estas especies químicas.
Deduzca la geometría de ambas moléculas.
Discuta la polaridad de cada una de las moléculas.
Ejercicio 3 · Bloque I
3Bloque I
2 puntosBloque IProblemas
En un laboratorio se dispone de los siguientes ácidos monopróticos: ácido cloroetanoico , ácido láctico , ácido propanoico , ácido etanoico .
Se mide el pH de una disolución de uno de los ácidos, obteniéndose un valor de . Teniendo en cuenta los datos suministrados, identifique de qué ácido se trata.
Una disolución del ácido más débil de los que figuran en la lista anterior tiene un pH . ¿Cuál es su concentración molar?
Ejercicio 3 · Bloque II
3Bloque II
2 puntosBloque IICuestiones
Se dispone en el laboratorio de láminas de plata, cobre y cinc, así como de disoluciones acuosas, de concentración , de las sales , y . Conteste razonadamente a las siguientes cuestiones:
¿Cuál de los tres metales es un reductor más fuerte?
Construimos una pila con un electrodo formado por una lámina de Ag metálica sumergida en la disolución de y otro formado por una lámina de Zn sumergida en la disolución de . ¿Cuál de los electrodos funciona como ánodo y cuál como cátodo de la pila? ¿Cuál es el potencial estándar de la pila formada?
Considerando la pila del apartado anterior, discuta si la lámina de cinc que actúa como electrodo aumenta o disminuye su masa a medida que avanza la reacción.
Ejercicio 4 · Bloque I
4Bloque I
2 puntosBloque IProblemas
En medio ácido, el peróxido de hidrógeno, , reacciona con el permanganato de potasio, , de acuerdo con la siguiente reacción (no ajustada):
Escriba la semirreacción de oxidación y la de reducción, así como la ecuación química global ajustada.
Para determinar el contenido en , de una muestra de agua oxigenada, que contenía un exceso de , se hicieron reaccionar con una disolución de de concentración . Se necesitaron de la disolución de para que la reacción se completase. Calcule la concentración de (en ) en el agua oxigenada analizada.
Ejercicio 4 · Bloque II
4Bloque II
2 puntosBloque IICuestiones
Se dispone en el laboratorio de cuatro disoluciones: A ( ), B ( ), C ( ) y D ( ). Discuta razonadamente si las siguientes afirmaciones son verdaderas o falsas:
El pH de la disolución A es mayor que el de la disolución C.
Al mezclar de la disolución A con de la disolución B se obtiene una disolución básica.
El pH de la disolución B es mayor que el de la disolución D.
Al mezclar de la disolución A con de la disolución D se obtiene una disolución neutra.
Ejercicio 5
5
2 puntosBloque IICuestiones
La cinética de la descomposición del peróxido de hidrógeno, , al reaccionar con el ion yoduro, , es de primer orden tanto respecto del como del . Discuta razonadamente si las siguientes afirmaciones son verdaderas o falsas:
Un aumento en la concentración de no tiene ningún efecto sobre la velocidad de reacción.
Al aumentar la temperatura a la que se produce la descomposición del peróxido de hidrógeno, aumenta la velocidad de la reacción.
La variación en la concentración del ion yoduro afecta más al valor de la velocidad de reacción que la variación de la concentración de .
La velocidad de la reacción se duplica al duplicar el volumen del reactor, manteniendo constante la temperatura.
Ejercicio 6
6
2 puntosBloque IICuestiones
Para cada una de las reacciones siguientes, escriba la fórmula de los reactivos orgánicos, complete las reacciones y nombre los compuestos orgánicos resultantes.
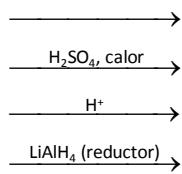
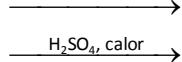
2-buteno (o but-2-eno) + bromuro de hidrógeno
3-pentanol (o pentan-3-ol)
1-butanol (o butan-1-ol) + ácido 2-metilpropanoico
Butanona
