Calcule cuántos moles de y han sobrado, así como la masa (en gramos) de obtenido.
QuímicaComunidad ValencianaPAU 2022Ordinaria
Química · Comunidad Valenciana 2022
10 ejercicios
Ejercicio 1 · Bloque I
1Bloque I
2 puntosBloque I
En la fabricación del ácido sulfúrico, una de las etapas consiste en transformar el en en virtud de la siguiente ecuación química:
Un reactor de litros contiene aire ( vol. y vol. ) a una presión total de y temperatura de . En dicho reactor se introducen moles de . La reacción, a esta temperatura, tiene un rendimiento del .
Calcule la presión parcial de cada uno de los gases de la mezcla final (, , y ) a la temperatura indicada, así como la presión total en el interior del reactor.
Ejercicio 1 · Bloque II
1Bloque II
2 puntosBloque II
Considere los elementos A, B, C y D, cuyos números atómicos son , , y , respectivamente. Responda razonadamente a las siguientes cuestiones:
Escriba la configuración electrónica en estado fundamental de cada uno de los elementos propuestos, e indique a qué grupo y periodo de la tabla periódica pertenece cada uno.
Ordene los elementos por orden creciente de su primera energía de ionización.
Indique el ion más estable que podría formarse a partir de cada uno de los cuatro elementos propuestos y escriba su configuración electrónica.
Deduzca la fórmula molecular del compuesto que se formaría entre los elementos A y B aplicando la regla del octeto y discuta el tipo de enlace que les une.
Ejercicio 2 · Bloque I
2Bloque I
2 puntosBloque I
Un reactor de litros a contiene una mezcla en equilibrio formada por de , de , de y un número indeterminado de moles de . La presión total del reactor es .
Calcule y para el equilibrio a .
Si se extraen del reactor los gases y en su totalidad, calcule la cantidad (en moles) de las cuatro sustancias una vez se haya alcanzado el nuevo equilibrio.
Ejercicio 2 · Bloque II
2Bloque II
2 puntosBloque II
Responda a las siguientes cuestiones sobre estructura molecular:
Dibuje las estructuras electrónicas de Lewis para las moléculas , y .
Indique razonadamente la geometría de las tres moléculas del apartado anterior y ordene de menor a mayor los ángulos de las moléculas ( del , del y del ).
Razone qué molécula/s del apartado (a) es/son polares.
Ejercicio 3 · Bloque I
3Bloque I
2 puntosBloque I
Se dispone de una disolución A de ácido clorhídrico comercial de densidad y riqueza en masa. Para preparar una segunda disolución B, se toman de la disolución A, diluyéndose con agua destilada hasta un volumen final de litros.
Calcule la concentración (en ) del ácido clorhídrico comercial (disolución A).
Calcule la concentración (en ) de la disolución B y su pH.
A de la disolución B, se añaden de una disolución de . Calcule el pH de la disolución final. Considere que los volúmenes son aditivos.
Ejercicio 3 · Bloque II
3Bloque II
2 puntosBloque II
Para el siguiente sistema en equilibrio en fase gaseosa: , responda razonadamente a las siguientes cuestiones:
Si se extrae del reactor parte del , ¿la relación aumenta, disminuye o permanece constante?
Se observa que al aumentar la temperatura se forma más . ¿La reacción es exotérmica o endotérmica?
Si se desea aumentar la cantidad de , manteniendo constante la temperatura, ¿se ha de aumentar o disminuir el volumen del reactor?
En un reactor a volumen y temperatura constantes se introducen inicialmente y . Razone si la presión total en el equilibrio será mayor, menor o igual que la inicial.
Ejercicio 4 · Bloque I
4Bloque I
2 puntosBloque I
A escala laboratorio, se pueden obtener pequeñas cantidades de cloro gaseoso mediante la reacción (no ajustada):
Escriba la semirreacción de oxidación y la de reducción, así como la ecuación química global ajustada.
Si se hace reaccionar de con un exceso de , ¿cuántos litros de se obtendrán, medidos a de presión y ?
Ejercicio 4 · Bloque II
4Bloque II
2 puntosBloque II
Responda a las siguientes cuestiones sobre química ácido-base:
Se dispone de tres disoluciones: una de , otra de y una tercera de , las tres a la misma concentración molar inicial del ácido. Razone cuál de estas disoluciones tendrá un mayor valor del pH.
Ordene justificadamente, de menor a mayor basicidad, las bases conjugadas de los tres ácidos anteriores.
Razone si la siguiente afirmación es verdadera o falsa: “El pH de una disolución de es igual al de una disolución de de igual concentración”.
Razone si la siguiente afirmación es verdadera o falsa: “Si a de una disolución de se les añaden de una disolución de , la mezcla final tendrá un pH neutro”.
Ejercicio 5
5
2 puntosBloque II
Responda a las siguientes cuestiones sobre reactividad y formulación orgánica:
Nombre los siguientes compuestos y razone cuál de ellos puede dar lugar a una cetona por oxidación.
Complete las siguientes reacciones químicas y nombre todos los compuestos orgánicos que se obtienen como productos en las mismas:
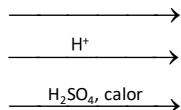
Ejercicio 6
6
2 puntosBloque II
Considere la reacción: . Se ha observado que, al duplicar la concentración de A, la velocidad de la reacción aumenta cuatro veces mientras que, al disminuir la concentración de B a la mitad, la velocidad disminuye en esa misma proporción.
Obtenga razonadamente la ley de velocidad de la reacción.
Cuando las concentraciones iniciales de A y B fueron y , respectivamente, la velocidad inicial de la reacción resultó ser . Calcule el valor de la constante de velocidad.
En las condiciones del apartado b), calcule la velocidad de desaparición de A y la velocidad de aparición de C.
Justifique por qué la velocidad de la reacción aumenta con la temperatura.
