Calcule la concentración de cada especie en el equilibrio.
QuímicaCastilla-La ManchaPAU 2023Ordinaria
Química · Castilla-La Mancha 2023
10 ejercicios
Ejercicio 1
1
3 puntosBloque A
En un recipiente de se introducen de y de , calentándose la mezcla a . Una vez alcanzado el siguiente equilibrio:
se analiza la mezcla, encontrándose que quedan moles de .
Calcule y a .
Justifique si una disminución del volumen del recipiente afectaría al equilibrio.
Ejercicio 2
2
3 puntosBloque A
Se añaden de amoniaco a la cantidad necesaria de agua para obtener de disolución.
Calcule el grado de disociación del amoniaco.
Calcule el pH de la disolución resultante.
Prediga que tipo de pH (sin cálculo numérico) presentará una disolución acuosa de cloruro amónico () y justifique la respuesta explicando los procesos químicos que tienen lugar.
Ejercicio 3
3
3 puntosBloque A
A la vista de los siguientes potenciales normales de reducción: y , razone si se desprenderá hidrógeno () cuando se introduce una barra de sodio en una disolución de ácido clorhídrico.
Se prepara una pila voltaica formada por electrodos estándar de y . Escriba la semirreacción que ocurre en cada electrodo indicando cuál es el cátodo y cuál el ánodo, así como la reacción global ajustada.
A la vista de los siguientes potenciales normales de reducción: y ¿Qué ocurrirá si se añaden limaduras de hierro (hierro en estado sólido) a una disolución de ? Justifique la respuesta indicando las semirreacciones que sucederán y la reacción global.
Ejercicio 4
4
3 puntosBloque A
Teniendo en cuenta los elementos A, B y C, con sus correspondientes números atómicos: , y , conteste razonadamente:
Cuáles pertenecen al mismo periodo y cuáles pertenecen al mismo grupo, indicando la identidad de los elementos a los que corresponden.
Cuál de los dos elementos B ó C tiene el primer potencial de ionización mayor y cual tiene un radio atómico mayor.
Deduzca la fórmula del compuesto que se formaría entre los elementos B y C indicando el tipo de enlace.
Escriba la combinación de números cuánticos para el último electrón del elemento B.
Ejercicio 5
5
2 puntosBloque B
Sabiendo que a , la solubilidad del en agua es :
Calcule la constante del producto de solubilidad () de dicha sal.
Calcule la solubilidad del en presencia de una disolución de .
Ejercicio 6
6
2 puntosBloque B
Dadas las siguientes moléculas: eteno (), etino () y metanol ():
Escriba sus estructuras de Lewis.
Indique la hibridación del átomo de carbono en estas moléculas, explicando el número de enlaces (sigma) y (pi).
Ejercicio 7
7
1 puntoBloque C
Para la reacción: , se ha calculado experimentalmente la expresión de la velocidad de reacción, la cual es . Justifique cómo se modifica la velocidad de reacción si:
Duplicamos la concentración de y se mantiene constante la de .
Se añade un catalizador positivo al medio.
Ejercicio 8
8
1 puntoBloque C
A una temperatura determinada, la para la descomposición del fluoruro de hidrógeno tiene un valor de . Al cabo de cierto tiempo se encuentran las siguientes concentraciones:
Justifique porqué el sistema no se encuentra en equilibrio.
¿Cómo ha de evolucionar el sistema para alcanzar el equilibrio?
Ejercicio 9
9
1 puntoBloque C
Justifique la veracidad o falsedad de las siguientes afirmaciones:
El cloruro de cesio es conductor de la electricidad mientras que un metal alcalino (ej. Sodio) no lo es.
El amoniaco () tiene un punto de ebullición más elevado que el del metano ().
Ejercicio 10
10
1 puntoBloque C
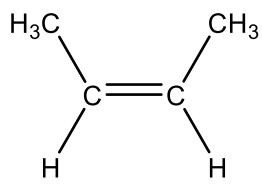
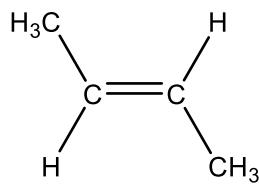
Indique que tipo de isomería presentan los siguientes pares de compuestos:
Los compuestos mostrados en las imágenes.