¿Se puede afirmar que este montaje permitirá el correcto funcionamiento del LED rojo?
QuímicaBalearesPAU 2018Extraordinaria
Química · Baleares 2018
10 ejercicios
Datos generales del examen
Ejercicio 1 · Opción A
1Opción A
1 puntoUn diodo emisor de luz (LED) es un dispositivo semiconductor que emite luz cuando se le aplica un voltaje determinado. La tecnología LED está muy extendida actualmente en iluminación, en medicina y en la industria de la automoción. Unos alumnos de Química quieren emplear una pila formada por electrodos de plata y plomo para el funcionamiento de un LED rojo que requiere un voltaje aproximado de - voltios.
Responde de forma justificada a las preguntas siguientes:

| Reacción | (V) |
En caso negativo, ¿qué combinación utilizarías de los electrodos indicados en la tabla 1 para que el LED pueda emitir luz roja? Indica la reacción redox global que tendría lugar ajustada.
Ejercicio 1 · Opción B
1Opción B
2,5 puntosEl reacciona con el según la siguiente reacción no ajustada:
Escribe y ajusta la reacción iónica y molecular por el método del ion-electrón.
¿Cuál es la especie oxidante? Justifica la respuesta.
Indica un procedimiento para prevenir la corrosión del hierro por la acción del medio ambiente.
Ejercicio 2 · Opción A
2Opción A
2,5 puntosEn un recipiente cerrado de dos litros de capacidad y vacío se introduce moles de gas fosgeno y se mantiene la temperatura a . Al alcanzar el siguiente equilibrio químico, se observa que la presión parcial de es de :
Calcula el valor de la constante de equilibrio, , a .
Calcula la presión total del sistema a .
Si se aumenta la presión de , ¿hacia dónde se desplazará el equilibrio químico? Razona la respuesta.
¿Se puede asegurar que, si se introduce inicialmente un catalizador dentro de la mezcla de reacción, se tardará más tiempo para alcanzar el equilibrio químico? Justifica la respuesta.
Ejercicio 2 · Opción B
2Opción B
2,5 puntosEn un laboratorio se dispone de una disolución de de concentración desconocida.
Determina la concentración del ácido sabiendo que el pH de la disolución es de .
Datos
Calcula el volumen de una disolución de que se necesita para preparar de una disolución de . Indica el material de vidrio que utilizarías en el laboratorio para preparar la disolución de .
En la ficha de seguridad química del aparece el siguiente pictograma. Indica su significado.

Ejercicio 3 · Opción A
3Opción A
2,5 puntosSe mezclan en un matraz aforado de con de agua destilada. Suponiendo que los volúmenes son aditivos, determina el pH de la disolución resultante.
Calcula el volumen necesario de una disolución de para neutralizar de . Sin hacer ningún cálculo numérico, razona si la disolución en el punto de equivalencia tendrá un pH ácido, básico o neutro.
Nombra el compuesto siguiente: .
Ejercicio 3 · Opción B
3Opción B
2 puntosLos valores de las energías reticulares de los compuestos y son, respectivamente, y . Justifica la diferencia entre los valores de la energía reticular del y . ¿Cuál de los dos compuestos presenta mayor dureza? Razona la respuesta.
Justifica la geometría de la molécula de mediante el modelo de la repulsión de pares de electrones de la capa de valencia. ¿Se puede afirmar que es una molécula apolar? Razona la respuesta.
Ejercicio 4 · Opción A
4Opción A
2,5 puntosSean los siguientes elementos: y .
Escribe la configuración electrónica del ion más estable del .
¿Cuál de los dos elementos presenta mayor energía de ionización? Justifica la respuesta.
¿Se puede afirmar que el radio del ion es más grande que el del ? Razona la respuesta.
Explica el tipo de enlace químico en el y en la molécula de .
Ejercicio 4 · Opción B
4Opción B
1,5 puntosEn un recipiente de volumen constante se genera a según la siguiente reacción ajustada:
¿Cómo afectaría al equilibrio químico una disminución del volumen total del recipiente? Justifica la respuesta.
Determina el valor de la constante a .
Si la temperatura se cambia a , ¿se puede afirmar que aumentará la formación de ? Razona la respuesta.
Ejercicio 5 · Opción A
5Opción A
1,5 puntosEn la siguiente figura se muestran tres isómeros de fórmula molecular . Responde razonadamente a las preguntas siguientes:
Indica el tipo de isomería que presentan las estructuras A y B.
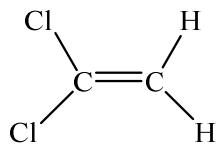
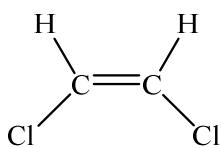
Indica el tipo de isomería que presentan las estructuras B y C.

Indica cuál es la hibridación de orbitales atómicos que presentan los átomos de carbono en la estructura C.
Ejercicio 5 · Opción B
5Opción B
1,5 puntosDada la siguiente reacción de adición de a un alqueno:
Nombra los compuestos y .
En general, ¿se puede afirmar que si aumentamos la concentración de los reactivos disminuirá la velocidad de reacción? Razona la respuesta.
