Indique el nombre y símbolo atómico del elemento.
QuímicaMurciaPAU 2023Ordinaria
Química · Murcia 2023
10 ejercicios
Ejercicio 1
1
2 puntosConsidere el elemento con , y un anión mononegativo de dicho elemento.
Indique el número de protones, neutrones y electrones del anión mononegativo, sabiendo que el isótopo más abundante de este elemento tiene una masa de .
Escriba la configuración electrónica del anión.
¿Qué elemento de la Tabla Periódica es isoelectrónico con dicho anión?
Razone cómo será el radio del anión, comparado con el del elemento (mayor, menor o igual).
Explique si los siguientes conjuntos de números cuánticos pueden corresponder a un electrón de un átomo de dicho elemento, en su estado fundamental:
i)
ii)
iii)
Ejercicio 2
2
2 puntosConsidere el gas metano y el gas butano y, basándose en las características de su enlace:
Indique qué tipo de compuestos son (metálicos, iónicos, covalentes atómicos o covalentes moleculares).
Razone cuál de ellos tendrá un mayor punto de ebullición.
Explique si serán conductores de la electricidad.
Explique cómo será su solubilidad en agua, comparada con la del amoníaco ().
Ejercicio 3
3
2 puntosConsidere el siguiente mecanismo de reacción, que consta de dos etapas elementales:
i) etapa lenta
ii) etapa rápida
Escriba la ecuación global para la reacción.
Escriba la ecuación de velocidad para la segunda etapa, e indique su orden de reacción.
Según el mecanismo propuesto, escriba la ecuación de velocidad para la reacción global.
Razone cómo variará la velocidad de la reacción global si se duplica la concentración de .
Indique si alguna de las especies involucradas en la reacción es un intermedio.
Explique, basándose en la cinética propuesta para las dos etapas, si la cantidad de presente durante el transcurso de la reacción será relativamente grande o pequeña.
¿Cómo afectará a la velocidad de reacción y a la constante de velocidad un aumento de ?
Ejercicio 4
4
2 puntosA la solubilidad () del en agua es .
Calcule el producto de solubilidad () del en agua, a .
Calcule el pH de una disolución saturada de en agua, a .
Explique si variará el pH (y cómo) si se adiciona de sólido a la disolución anterior.
Si a de agua a se adicionan de una disolución de , y de una disolución de , justifique numéricamente si precipitará .
Ejercicio 5
5
2 puntos de una disolución de se mezclan con de una disolución de . La disolución así obtenida tiene . Calcule la concentración de la disolución inicial de .
Se valoran de la disolución de del apartado anterior con el del apartado anterior. Si se llena la bureta con del , razone si serán suficientes para llegar al punto de equivalencia. (NOTA: este apartado puede contestarse sin conocer el resultado del anterior).
Ejercicio 6
6
2 puntosCalcule el pH de una disolución de (), de concentración .
Explique cómo variará el pH (aumentará, disminuirá o permanecerá igual), si a de la disolución anterior se le adicionan de una disolución de .
¿Cuál será la concentración de iones en la disolución resultante del apartado b?
Ejercicio 7
7
2 puntosDada la siguiente reacción de oxidación-reducción (sin ajustar):
Indique cuál es el agente oxidante y el reductor, y cómo varía su estado de oxidación.
Ajuste las semirreacciones de oxidación y reducción, indicando los electrones intercambiados.
Escriba la reacción global completamente ajustada.
Ejercicio 8
8
2 puntosSe realiza la electrolisis de una disolución acuosa de empleando dos electrodos de grafito. En uno de ellos se deposita y en el otro se desprende un gas. Teniendo en cuenta que el agua puede sufrir los siguientes procesos redox: y y que ni el grafito ni el nitrato participan en la reacción, conteste a las siguientes cuestiones:
¿En qué electrodo (cátodo o ánodo) se depositará la ? Escriba esta semirreacción ajustada.
Explique qué gas se deprenderá en el otro electrodo y escriba la semirreacción correspondiente, así como la reacción global de la celda electrolítica. NOTA: no se necesitan los potenciales redox.
¿Cuántos moles de se habrán depositado al cabo de de electrolisis, si la corriente aplicada es de ? NOTA: no se necesita el peso atómico de la para contestar.
Ejercicio 9
9
2 puntosEscriba las fórmulas semidesarrolladas de los siguientes pares de compuestos e indique el tipo y subtipo de isomería que presentan entre sí:
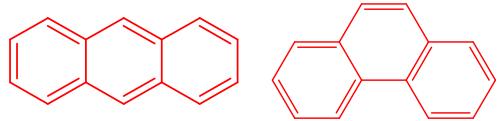
i) antraceno y fenantreno
ii) pentan-3-ona y pent-2-en-3-ol
Indique el tipo y subtipo de isomería que presenta el siguiente par de compuestos:
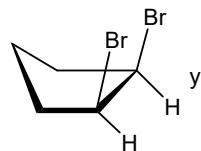
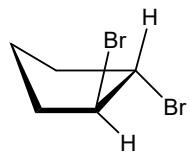
Indique el tipo de reacción orgánica (una sola palabra es suficiente):
Nombre las dos sustancias orgánicas que intervienen en la reacción anterior.
Ejercicio 10
10
2 puntosFormule o nombre:
i)
ii) N-propilformamida
Escriba las fórmulas semidesarrolladas del anisol y el fenilmetanol e indique el tipo y subtipo de isomería que presentan entre sí estos dos compuestos.
Indique el tipo y subtipo de isomería que presenta el siguiente par de compuestos:
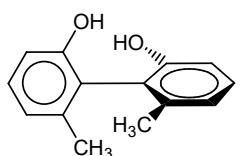
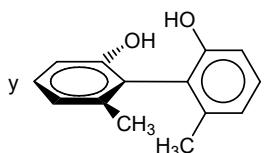
Complete las siguientes reacciones orgánicas, según el tipo de reacción indicado:
i) Oxidación:
ii) Sustitución (electrófila aromática) (dos productos):
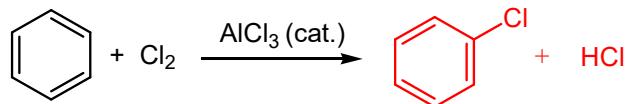
Nombre los reactivos orgánicos de partida en las dos reacciones anteriores.
