Represente el ciclo de Born-Haber para el y señale la dependencia de la energía reticular con respecto a la carga de los iones y al radio de los mismos.
QuímicaLa RiojaPAU 2024Extraordinaria
Química · La Rioja 2024
10 ejercicios
Ejercicio 1
1
2 puntosDados dos átomos con la siguiente configuración electrónica: y :
¿Qué molécula se formará favorablemente: o ? Razone su respuesta.
Justifique la geometría de la molécula formada y su polaridad.
Ejercicio 2
2
2 puntosPara el siguiente equilibrio químico:
la constante de equilibrio es igual a a una temperatura de
Si se introducen de , de y de en un recipiente de y se calienta a , ¿la reacción se desplazará hacia la formación de productos o de reactivos? Razone su respuesta
Calcule las concentraciones de , y tras alcanzar cuando se calientan a , de en un recipiente de .
Calcule la del equilibrio.
Ejercicio 3
3
2 puntosDada la pila electroquímica
Ajuste la reacción química en forma iónica de la reacción que ocurre en la pila.
Calcule el potencial estándar de la pila y la variación de energía libre en condiciones estándar ().
Dibuje un esquema de la pila, indicando todos los elementos necesarios y la polaridad de los electrodos.
Ejercicio 4
4
2 puntosSe prepara una disolución de mediante la dilución de de una disolución de ácido nítrico () en el agua necesaria para llegar hasta dicho volumen total. Calcule:
El pH de esta nueva disolución.
La concentración necesaria de ácido metanoico () para que una disolución tenga el mismo el mismo pH que la disolución del apartado a).
El volumen necesario de ácido metanoico comercial, de concentración y densidad , para preparar de una disolución con .
Ejercicio 5
5
2 puntosIdentifique y nombre correctamente (0,5 puntos por apartado):
Un isómero de cadena del compuesto .
Un isómero de posición del compuesto .
Un isómero de función del compuesto: .
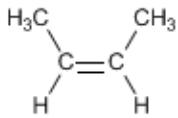
Un isómero espacial geométrico del compuesto mostrado en la imagen.
Ejercicio 6
6
2 puntosRazone, en función al tipo de enlace que presentan las siguientes especies, la veracidad o falsedad de las siguientes afirmaciones:
El fluoruro de potasio () es soluble en agua.
El aluminio no conduce la electricidad y es un mal conductor térmico.
El metano () tiene un punto de fusión más alto que el amoniaco ().
Los sólidos de red covalente, como el diamante, presentan un punto de fusión muy alto.
Ejercicio 7
7
2 puntosLa velocidad de reacción, a una temperatura de , de la descomposición de en y se duplica al duplicar la concentración inicial de .
Determine la expresión de la ecuación de velocidad y el orden de reacción.
Si se introducen de en un recipiente de , la velocidad de reacción es . Determine la constante de velocidad y sus unidades.
Si en esas mismas condiciones se introducen de , indique, razonadamente, cómo variará la constante de velocidad y la velocidad de reacción inicial.
Ejercicio 8
8
2 puntosDada la siguiente reacción química:
Deduzca, razonadamente, la veracidad o falsedad de los siguientes enunciados:
Cuando se alcanza el equilibrio químico para cualquier proporción inicial de gases, la concentración es siempre el doble que la concentración .
A temperatura constante, el equilibrio se desplazará hacia la formación de producto cuando se aumenta la presión del sistema.
Cuando se alcanza el equilibrio químico, la disminuirá a la mitad cuando se añade al sistema el doble de .
Sabiendo que la reacción directa es exotérmica, el equilibrio se desplazará hacia la formación de reactivos cuando calentamos el sistema.
Ejercicio 9
9
2 puntosEl hidróxido de cobre(II) () es un compuesto poco soluble en agua, cuya solubilidad molar es a .
Calcule el producto de solubilidad de dicho compuesto.
Calcule el pH de una disolución saturada de dicho compuesto.
Calcule la solubilidad, en , del hidróxido de cobre(II), al añadir dicho compuesto a una disolución acuosa de cuyo pH inicial es .
Si se añade un ácido fuerte a una disolución saturada de hidróxido de cobre(II), razone, cualitativamente, si se disolverá o precipitará más cantidad de dicho compuesto.
Ejercicio 10
10
2 puntosDados los compuestos orgánicos: , y :
Nombre correctamente dichos compuestos.
Proponga una reacción orgánica para cada uno de los compuestos anteriores, identificando el tipo de reacción y los productos.
Identifique un alcano con isomería óptica y dibuje sus dos isómeros.
