Escriba sus nombres y sus configuraciones electrónicas e indique para cada uno de ellos el grupo y periodo de la Tabla Periódica al que pertenece, y cómo se suele denominar dicho grupo.
QuímicaMurciaPAU 2024Ordinaria
Química · Murcia 2024
10 ejercicios90 min de duración
Ejercicio 1
1
2 puntosDados los elementos () y ():
Indique en qué estado (sólido, líquido o gas) se presentará cada uno de esos elementos en condiciones normales (, ) y si conducirá, o no, la electricidad.
Explique brevemente cuál de ellos tendrá mayor afinidad electrónica (AE), cuál mayor energía de ionización (EI) y cuál mayor radio.
Ejercicio 2
2
2 puntosConsidere las siguientes sustancias orgánicas: metanol (), etilenglicol () y glicerol (glicerina ), que son alcoholes líquidos a temperatura ambiente.
Represente sus estructuras de Lewis y en base a ellas indique cómo será la geometría en torno a los átomos de y de estas moléculas.
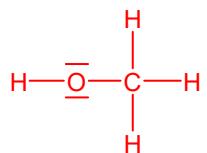
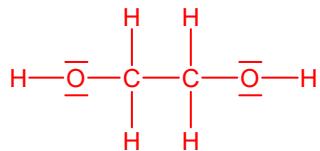
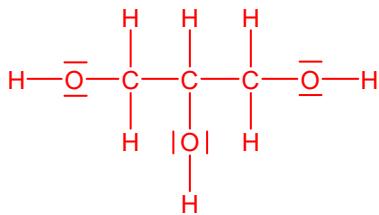
Indique qué tipo de enlace intermolecular será predominante entre las moléculas en estas sustancias, y ordénelas por orden creciente de punto de ebullición.
Explique brevemente si en condiciones normales serán conductoras de la electricidad.
Explique brevemente si estas tres sustancias serán miscibles entre sí y con el agua.
Ejercicio 3
3
2 puntosLa piedra caliza está compuesta mayoritariamente por que descompone al calentar según la siguiente reacción:
Indique qué sustancias de la reacción anterior son óxidos, y nómbrelos.
Explique brevemente si se trata, o no, de una reacción redox.
Observando la ecuación química, explique si la entropía aumenta o disminuye.
Calcule la del .
Si una muestra de de piedra caliza contiene un de , calcule el volumen de que se formará en su descomposición, en condiciones normales ( y ).
Ejercicio 4
4
2 puntosEn un recipiente de se introducen de y de , alcanzándose el siguiente equilibrio:
Una vez alcanzado el equilibrio, a una determinada temperatura, la concentración de es .
Nombre el producto de esta reacción ().
¿Cuál será la concentración de en el equilibrio, a esa temperatura? NOTA: no es necesario conocer el valor de la constante de equilibrio para contestar esta cuestión.
Si se aumenta la temperatura en , explique brevemente si:
cambiará el valor de la constante de equilibrio.
la concentración de aumentará, disminuirá o permanecerá constante.
Si a una temperatura de , calcule el valor de a esa temperatura.
Ejercicio 5
5
2 puntosUn bidón contiene de una disolución de (un ácido fuerte), de concentración .
Escriba la reacción de disociación de este ácido, y nombre el ácido y su base conjugada.
Calcule el pH de la disolución.
Indique la cantidad, en moles, de protones presentes en de dicha disolución.
Calcule los moles de presentes en de dicha disolución, y el pH en esos .
Si se toma de dicha disolución y se diluye hasta , en otro bidón, ¿cuál será la concentración, en molaridad, de la nueva disolución así preparada?
¿Cuál sería el pH de una disolución de ?
Ejercicio 6
6
2 puntosUn bidón contiene de una disolución de . Se mide el pH y resulta ser igual a .
Escriba la reacción de disociación de este ácido y explique numéricamente, basándose en el dato de concentración y el pH medido, si se trata de un ácido fuerte o débil.
Nombre el ácido y su base conjugada.
Calcule el grado de disociación del ácido, expresándolo con una única cifra significativa.
Calcule la del ácido.
Si se vacía la mitad del bidón, ¿cómo será la concentración de la disolución en su interior?
Ejercicio 7
7
2 puntosDada la siguiente reacción de oxidación-reducción:
Nombre los compuestos , , y .
Indique cuál es el agente oxidante y el reductor, y como varían sus números de oxidación.
Ajuste la reacción mediante el método del ion-electrón.
Ejercicio 8
8
2 puntosUna corriente de circula durante por una celda electrolítica que contiene una disolución de en . Conteste a las siguientes cuestiones, teniendo en cuenta las semirreacciones:
¿Qué iones habrá en la disolución? (considerando también la autoionización del agua).
Escriba y ajuste la semirreacción del cátodo, indicando qué gas se desprende.
¿Qué gas (, o ) se desprenderá en el ánodo? Razone su respuesta.
¿Qué volumen de se desprenderá durante la electrolisis, a y ?
Si la fuera , razone si se desprendería el doble de durante el mismo tiempo.
Ejercicio 9
9
2 puntosObserve las siguientes parejas de compuestos orgánicos, todos ellos de fórmula molecular .
(NOTA: se recomienda escribir sus fórmulas semidesarrolladas, para contestar las siguientes cuestiones)
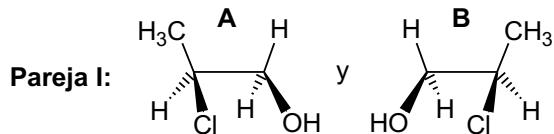
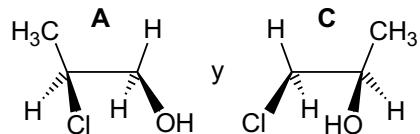
Explique brevemente si los tres compuestos, A, B y C, son isómeros entre sí.
Explique brevemente si los compuestos A, B y C tienen algún carbono asimétrico.
Explique brevemente el tipo y subtipo de isomería que presenta cada pareja.
Indique de qué tipo es la siguiente reacción a partir de A, y nombre el producto orgánico formado:
Ejercicio 10
10
2 puntosEscriba las fórmulas semidesarrolladas de los siguientes pares de compuestos orgánicos e indique el tipo y subtipo de isomería que presentan entre sí:
metil vinil éter y prop-2-en-1-ol
isopropilbenceno y propilbenceno
Nombre los siguientes compuestos, distinguiéndolos según su isomería, e indique de qué tipo y subtipo de isomería se trata:
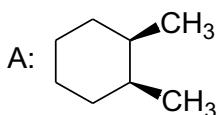
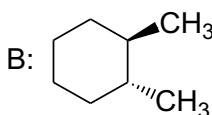
Complete la siguiente reacción de nitración (sustitución electrófila aromática), y nombre el compuesto orgánico que se forma:
