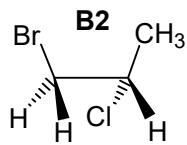
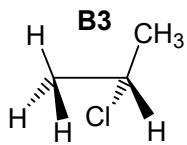
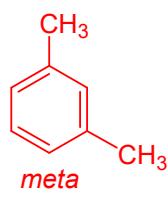
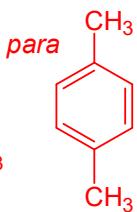
Indique, en cada caso, cuál de ellos (pueden repetirse elementos):
Es un metal alcalinotérreo.
No presenta afinidad electrónica.
Es el más electronegativo.
Tiene el mayor radio atómico.
Presenta como números de oxidación importantes +3 y +5.
Al ganar dos electrones, es isoelectrónico con el Kr.