Calcule el calor producido a presión constante al hacer explotar de TNT en condiciones estándar y a .
QuímicaCataluñaPAU 2017Ordinaria
Química · Cataluña 2017
14 ejercicios
Ejercicio 1 · Serie 1
1Serie 1
2 puntosSerie 1
El trinitrotolueno (TNT) es un explosivo muy potente que, en relación con la nitroglicerina, tiene la ventaja de que es más estable en caso de impacto, golpes o fricción. La descomposición explosiva del TNT se puede representar mediante la ecuación química siguiente:
Justifique si la variación de entropía estándar de esta reacción es positiva o negativa, y cómo influye la temperatura en la espontaneidad de esta reacción. Suponga que la entalpía y la entropía no varían en función de la temperatura.
Ejercicio 1 · Serie 5
1Serie 5
2 puntosSerie 5
El hidróxido de magnesio, , es un antiácido que se utiliza para aliviar los síntomas de indigestión o acidez.
Escriba la reacción del equilibrio de solubilidad del hidróxido de magnesio en agua y calcule su solubilidad a , en , si el pH de la solución saturada es igual a .
¿Qué efecto tendrá la adición de una solución acuosa de cloruro de magnesio () en la solubilidad del hidróxido de magnesio? ¿Y la adición de una solución acuosa de ácido clorhídrico ()? Justifique las respuestas.
Ejercicio 2 · Serie 1
2Serie 1
2 puntosSerie 1
Las reacciones redox se utilizan en muchos procesos de la química: para generar energía eléctrica (pila), para provocar reacciones químicas que no son espontáneas (electrólisis) o para obtener sustancias de gran interés.
Un grupo de estudiantes quiere montar una pila en el laboratorio, en condiciones estándar y a . La pila tiene la notación siguiente:
Explique el procedimiento experimental que deberán seguir para construir esta pila y medir su fuerza electromotriz, e indique el material y los reactivos que necesitarán.
En otro experimento, los estudiantes disponen de dos vasos de precipitados, cada uno de los cuales contiene una solución de nitrato de cobre(II), a . En el primero, introducen una lámina de zinc, y en el segundo, un hilo de plata. Justifique si habrá reacción o no en cada uno de los vasos; en caso afirmativo, escriba la reacción ajustada.
Ejercicio 2 · Serie 5
2Serie 5
2 puntosSerie 5
Una de las utilidades de la electrólisis es la obtención de algunos metales. Por ejemplo, el magnesio se obtiene industrialmente por electrólisis del cloruro de magnesio () procedente de salmueras o del agua de mar. En esta electrólisis, el cloruro de magnesio se encuentra en estado líquido o fundido.
Escriba las semirreacciones que tienen lugar en cada uno de los electrodos durante el proceso de electrólisis del cloruro de magnesio fundido, y también la reacción iónica global. Indique el nombre y la polaridad de los electrodos.
Calcule la masa de magnesio que obtendremos si hacemos pasar una corriente eléctrica de durante .
Ejercicio 3 · Serie 1
3Serie 1
2 puntosSerie 1
El ozono, una sustancia que actúa como filtro de las radiaciones solares, se puede descomponer en oxígeno en la estratosfera mediante un proceso exotérmico que consta de las dos etapas elementales siguientes:
Etapa 1:
Etapa 2:
Escriba la reacción global del proceso de descomposición del ozono. Realice una representación gráfica aproximada que muestre la energía en función de la coordenada de reacción, y señale las energías de activación y la variación de entalpía de la reacción.
A partir del modelo del estado de transición (o complejo activado), explique el concepto energía de activación y justifique cuál de las dos etapas de la descomposición del ozono es más lenta.
Ejercicio 3 · Serie 5
3Serie 5
2 puntosSerie 5
El cloruro de amonio () es una sal de color blanco que tiene un efecto expectorante. También tiene aplicaciones como diurético y como agente acidulante.
Determine el pH a de un medicamento que se prepara disolviendo de clorur de amonio en de solución.
Explique cómo prepararía en el laboratorio el medicamento del apartado anterior. Indique las operaciones que realizaría y el nombre de todo el material de laboratorio que utilizaría.
Ejercicio 4 · Serie 1
4Serie 1
2 puntosSerie 1
Elija UNA cuestión entre la 4 y la 5.
Experimentalmente, hemos llevado a cabo el seguimiento de la reacción en fase gaseosa siguiente, en un recipiente cerrado y a una temperatura de :
En el gráfico siguiente podemos ver los cambios de concentración de las tres sustancias gaseosas A, B y C, en función del tiempo.
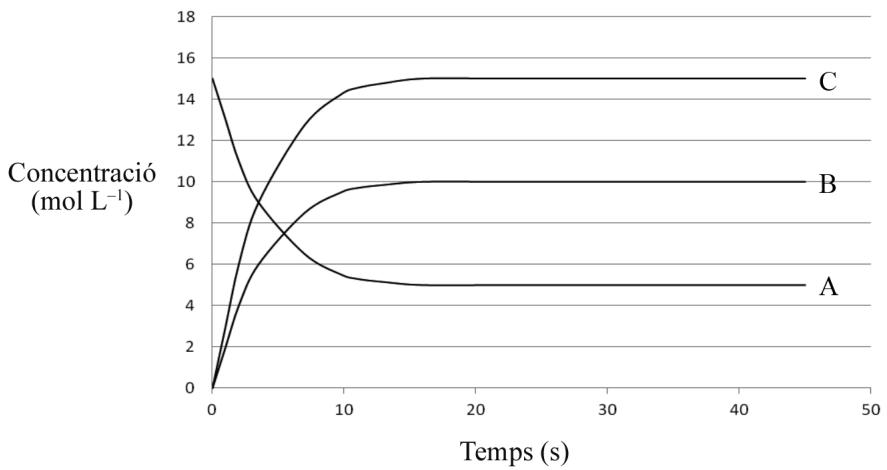
Justifique cuáles serán las concentraciones de las sustancias A, B y C en el equilibrio, y calcule la constante de equilibrio en concentraciones () y la constante de equilibrio en presiones () de esta reacción a .
Tenemos las sustancias A, B y C en equilibrio a . ¿Cómo se modificarán la constante de equilibrio en concentraciones y la masa de la sustancia A si aumentamos el volumen del recipiente pero mantenemos la temperatura? Razone las respuestas.
Ejercicio 4 · Serie 5
4Serie 5
2 puntosSerie 5
Elija UNA cuestión entre la 4 y la 5.
El bioetanol es un biocombustible que se obtiene por fermentación de los azúcares presentes en las especies vegetales que tienen un alto contenido en sacarosa, como por ejemplo la caña de azúcar o la remolacha, o bien un alto contenido en almidón, como por ejemplo el trigo, el maíz, la cebada o las patatas. El bioetanol se puede utilizar como combustible en vehículos de motor.

| Compuesto | (kJ mol) |
| -285,8 | |
| -393,5 | |
| -277,6 |
Escriba y ajuste la reacción de combustión del etanol, y calcule la variación de entalpía estándar a y la variación de energía interna estándar a del proceso de combustión.
Calcule el calor liberado, a y , asociado a la combustión de de etanol, de densidad . Razone si la variación de entropía en condiciones estándar, asociada a la combustión del etanol, es positiva o negativa.
Ejercicio 5 · Serie 1
5Serie 1
2 puntosSerie 1
Elija UNA cuestión entre la 4 y la 5.
El bromometano (o bromuro de metilo) se utilizó como plaguicida hasta que se empezó a prohibir en muchos países, a partir del año 2000, por el hecho de que genera radicales de bromo (Br) que participan en el proceso de reducción de la capa de ozono en la estratosfera. En esta capa de la atmósfera puede tener lugar la reacción de fotodisociación siguiente:
Calcule la frecuencia y la longitud de onda de la radiación electromagnética capaz de romper el enlace C—Br en una molécula de bromometano.
Defina el término orbital atómico según el modelo ondulatorio del átomo. Escriba la configuración electrónica del átomo de bromo e indique los números cuánticos del electrón más externo de este átomo.
Ejercicio 5 · Serie 5
5Serie 5
2 puntosSerie 5
Elija UNA cuestión entre la 4 y la 5.
Cuando se produce la lluvia ácida, uno de los pasos intermedios de formación de ácido sulfúrico en la atmósfera es la reacción entre el dióxido de azufre y el oxígeno, que genera trióxido de azufre. La reacción ajustada es la siguiente:
La reacción es exotérmica y la constante de equilibrio en presiones a es .
Un recipiente cerrado de a contiene de dióxido de azufre, de oxígeno y de trióxido de azufre. Explique justificadamente si la mezcla gaseosa se encuentra en equilibrio y cómo evolucionará con el tiempo.
¿Qué efectos tendrá una disminución de la temperatura en el equilibrio y en la constante de equilibrio ? ¿Y una disminución de la presión total?
Ejercicio 6 · Serie 1
6Serie 1
2 puntosSerie 1
Elija UNA cuestión entre la 6 y la 7.
La salinidad de las aguas oceánicas determina las condiciones de vida de los organismos marinos y varía en función de las características de cada océano. La determinación de la salinidad se lleva a cabo midiendo un parámetro del agua de mar, como por ejemplo la conductividad eléctrica o la concentración de ion cloruro. Este último parámetro se mide mediante una valoración del ion cloruro con nitrato de plata :
Cuando hemos valorado de agua de mar, hemos necesitado de una solución de nitrato de plata para poder llegar al punto final de la valoración. Calcule la salinidad del agua de mar, expresada como concentración de en .
Escriba la ecuación del equilibrio de solubilidad del cloruro de plata y determine su solubilidad a , expresada en . Justifique si la solubilidad del cloruro de plata aumenta, disminuye o se mantiene en una solución acuosa concentrada de .
Ejercicio 6 · Serie 5
6Serie 5
2 puntosSerie 5
Elija UNA cuestión entre la 6 y la 7.
El smog fotoquímico (photochemical smog) es una mezcla de humo y niebla que produce, entre otros efectos, irritación ocular. Uno de los principales irritantes oculares del smog es el formaldehído , que se produce por una reacción entre el etileno y el ozono , según la ecuación química siguiente:
Hemos realizado diferentes experimentos, a , para determinar la velocidad inicial de reacción a diferentes concentraciones y hemos obtenido los resultados siguientes:
| Experimento | [] (mol L) | [] (mol L) | Velocidad (mol Ls) |
| 1 | |||
| 2 | |||
| 3 |
Determine el orden de reacción de cada reactivo y el orden total.
Calcule la constante de velocidad de la reacción a . ¿Qué influencia tiene un aumento de la temperatura sobre la velocidad de reacción? Justifique la respuesta teniendo en cuenta la teoría de las colisiones.
Ejercicio 7 · Serie 1
7Serie 1
2 puntosSerie 1
Elija UNA cuestión entre la 6 y la 7.
El ácido metanoico (), llamado habitualmente ácido fórmico, se puede obtener de las hormigas. Cuando una hormiga nos pica, nos inyecta aproximadamente de ácido fórmico puro, y este líquido que nos ha inyectado se mezcla con de agua de nuestro cuerpo.

Calcule la concentración de la solución acuosa de ácido fórmico que se forma en nuestro cuerpo cuando nos pica una hormiga, expresada en . ¿Qué pH tendrá esta solución?
Para neutralizar las picaduras de hormiga, podemos utilizar hidrogenocarbonato de sodio (). Escriba la reacción de neutralización y calcule la masa de necesaria para neutralizar el ácido fórmico que nos inyecta una hormiga cuando nos pica.
Ejercicio 7 · Serie 5
7Serie 5
2 puntosSerie 5
Elija UNA cuestión entre la 6 y la 7.
Las energías de ionización nos ayudan a entender algunas diferencias cualitativas entre estructuras electrónicas de diferentes átomos. La tabla siguiente muestra los valores de la primera energía de ionización del litio, el berilio y el boro.
| Elemento | Primera energía de ionización (kJ mol) |
| Li | 520,3 |
| Be | 899,5 |
| B | 800,6 |
Explique justificadamente la diferencia que hay entre los valores de la primera energía de ionización de los tres átomos.
Calcule la frecuencia mínima y la longitud de onda máxima de la radiación que puede ionizar los átomos de litio gaseoso en estado fundamental.
