¿Qué pH tendrá la disolución resultante de esta mezcla?
QuímicaAragónPAU 2021Extraordinaria
Química · Aragón 2021
10 ejercicios
Ejercicio 1
1
2 puntosSe toman de una disolución de de y se le añade de .
¿Qué cantidad exacta de habría que haber añadido para que el pH de la disolución fuera neutro?
Ejercicio 2
2
2 puntosIndique razonadamente en qué condiciones de temperatura (altas, bajas o a cualquier temperatura) serán espontáneas las siguientes reacciones, o si hay alguna que no será espontánea a ninguna temperatura:
Ejercicio 3
3
2 puntosEl reacciona con hipoclorito de potasio, , en medio de ácido sulfúrico, para dar , , y agua.
Ajuste la ecuación iónica por el método del ión-electrón y escriba la ecuación molecular completa. Indique el agente oxidante y el reductor.
¿Qué volumen de una disolución de permanganato de potasio reaccionará completamente con de otra disolución que contiene de hipoclorito de potasio por litro?
Ejercicio 4
4
2 puntosObserve las siguientes distribuciones de electrones de átomos neutros y conteste razonadamente a las preguntas:
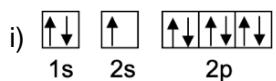
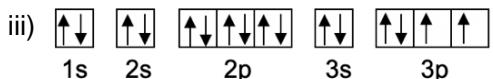
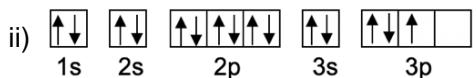
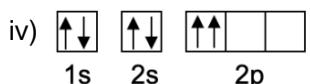
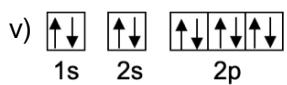
¿Cuáles de estos diagramas muestran una distribución electrónica posible y cuáles no?
De entre todos los diagramas hay uno que representa un estado excitado. ¿Cuál es? Escriba la configuración electrónica de su estado fundamental e indique de qué elemento se trata, así como el periodo y el grupo al que pertenece.
¿Cuál de todas las distribuciones electrónicas representa a un gas noble? Escriba los números cuánticos de todos los electrones de la última capa de este elemento.
Ejercicio 5
5
2 puntosLa solubilidad del cromato de plata es de por cada .
Escriba el equilibrio de solubilidad del cromato de plata y calcule el valor del producto de solubilidad.
¿Precipitará el cromato de plata cuando se mezclen de una disolución de cromato de sodio y de una disolución de nitrato de plata?
Ejercicio 6
6
2 puntosEl pentacloruro de antimonio es un líquido viscoso de densidad , el cual al elevar la temperatura se descompone de acuerdo con el siguiente equilibrio:
En un recipiente de se introducen de pentacloruro de antimonio y se calienta a , observándose que, al alcanzar el equilibrio, la presión del sistema es de .
Calcule los moles de cada especie en el equilibrio.
Calcule el valor de .
¿Cómo evolucionará el equilibrio si la presión total del sistema se reduce a la mitad?
Ejercicio 7
7
2 puntosDadas las siguientes sustancias: , , y .
¿Qué tipo de enlace (iónico, covalente o metálico) está presente en estas sustancias? Justifique la respuesta.
Para las moléculas anteriores que presenten enlaces covalentes, explique sus estructuras de Lewis y razone su geometría según la teoría de repulsión de pares de electrones de la capa de valencia (TRPECV). ¿Qué puede decir sobre la polaridad de estas moléculas?
Ejercicio 8
8
2 puntosConteste razonadamente:
¿Qué ocurrirá si se añade una disolución de sulfato de cobre(II) a un recipiente de ? ¿Y si el recipiente es de ?
¿En qué sentido, hacia la derecha o hacia la izquierda, se producirán espontáneamente las siguientes reacciones?
Ejercicio 9
9
2 puntosLa combustión de butano gaseoso a conduce a la obtención de dióxido de carbono (gas) y agua líquida, y la entalpía molar estándar de esta reacción es .
Escriba y ajuste la ecuación de combustión de butano.
Con los datos proporcionados, calcule la entalpía molar de formación del butano.
¿Cuánto calor se pondrá en juego si se hacen reaccionar de butano con de oxígeno?
Ejercicio 10
10
2 puntosEscriba la base conjugada de los siguientes ácidos de Brönsted: , , , . ¿Alguna de estas especies se puede comportar también como una base? Justifique las respuestas.
El tiene una y el ácido acético tiene una , ¿cuál de los dos ácidos es más débil? ¿cuál de ellos tendrá una base conjugada más fuerte? Justifique las respuestas.
