Determina el peso molecular de la alanina.
QuímicaBalearesPAU 2025Extraordinaria
Química · Baleares 2025
9 ejercicios90 min de duración
Ejercicio 1
1
2 puntosEl premio Nobel de Química del año 2024 fue concedido conjuntamente al investigador David Baker, por el diseño computacional de proteínas, y a los investigadores Demis Hassabis y John M. Jumper, por la predicción de la estructura de proteínas (figura 1). Uno de los aminoácidos que forman parte de las proteínas de los seres vivos es la alanina (figura 2).

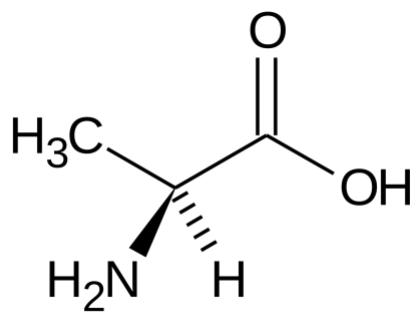
Identifica dos grupos funcionales presentes en la molécula de la alanina.
Formula o nombra los compuestos siguientes:
Ácido nítrico
En el laboratorio, se pretende valorar un ácido débil monoprótico del tipo de concentración desconocida con una disolución de . Explica el procedimiento experimental que seguirías para llevar a cabo la valoración ácido-base.
Ejercicio 2 · Opción A
2Opción A
2 puntosContesta solo uno de los dos apartados: 2A o 2B.
El ácido hipocloroso () es considerado un desinfectante muy potente y, por este motivo, es ampliamente utilizado para la desinfección en muchos centros sanitarios a raíz de la covid. Este ácido, muy a menudo, se utiliza en disoluciones de concentración .
Calcula la constante de acidez del ácido hipocloroso, sabiendo que a una disolución acuosa de este ácido tiene un pH de .
Se valoran de una disolución de con una disolución de hidróxido de sodio () de concentración .
Escribe la reacción de neutralización del ácido hipocloroso.
Calcula el volumen de necesario para alcanzar el punto de equivalencia en la valoración anterior.
Ejercicio 2 · Opción B
2Opción B
2 puntosContesta solo uno de los dos apartados: 2A o 2B.
La molécula de dicloro () en estado gaseoso es un compuesto de gran importancia en la industria química. Uno de los métodos de obtención de dicloro gaseoso es a partir de la oxidación de ácido clorhídrico () con ácido nítrico (). Se obtienen, además del , y agua.
Escribe y ajusta por el método del ion-electrón la reacción química, en forma iónica, que tiene lugar en este proceso.
Calcula el volumen de , en litros, que se obtendrá, a y a , si se hacen reaccionar de una disolución de con en exceso, suponiendo un rendimiento de la reacción del .
Ejercicio 3 · Opción A
3Opción A
2 puntosContesta solo uno de los dos apartados: 3A o 3B.
Considera las especies siguientes: , , y .
Selecciona la especie química que:
presenta interacciones de van der Waals y es un gas a temperatura ambiente;
presenta una elevada conductividad eléctrica cuando se encuentra en estado sólido;
presenta interacciones tipo enlace de hidrógeno y se encuentra en estado líquido a temperatura ambiente;
es buen conductor de la electricidad cuando se encuentra en disolución, pero es muy mal conductor en estado sólido.
En todos los casos justifica, de manera razonada, la elección de la especie química seleccionada.
Ejercicio 3 · Opción B
3Opción B
2 puntosContesta solo uno de los dos apartados: 3A o 3B.
Dados los iones y , justifica si las afirmaciones siguientes son verdaderas o falsas:
Los dos iones tienen el mismo número de protones.
Estas dos especies son isoelectrónicas.
Los dos iones son isótopos del neón ().
La molécula es apolar.
Ejercicio 4 · Opción A
4Opción A
2 puntosContesta solo uno de los dos apartados: 4A o 4B.
El óxido de cobre (I) () fue la primera sustancia utilizada como semiconductor antes de la implantación de los derivados del silicio. Actualmente todavía tiene múltiples aplicaciones industriales como pigmento, fungicida, antiincrustante, etc. Este compuesto se puede obtener a partir de la descomposición del óxido de cobre (II) () mediante la siguiente reacción química ajustada:
En un recipiente, inicialmente vacío, de de capacidad, se introducen de y se calienta hasta una temperatura de ; cuando se alcanza el equilibrio químico, la presión total dentro del recipiente es de .
Calcula los moles de que se habrán formado.
Calcula los valores de y .
Si el mismo proceso se repite dentro de un recipiente de de capacidad, manteniendo todos los otros parámetros constantes, ¿se obtendrá más o menos cantidad de ? Justifica la respuesta.
Ejercicio 4 · Opción B
4Opción B
2 puntosContesta solo uno de los dos apartados: 4A o 4B.
Formula los compuestos siguientes:
pentanal
pentan-2-ona
Indica, de manera razonada, para cada par de compuestos orgánicos, si estos compuestos son isómeros. En caso afirmativo, explica el tipo de isomería que se da en cada uno de los casos:
n-butano y 2-metilpropano
1-cloropropano y 2-cloropropano
etanol y etanal
Ejercicio 5 · Opción A
5Opción A
2 puntosContesta solo uno de los dos apartados: 5A o 5B.
El metanol (), además de ser empleado para la síntesis de otros compuestos químicos, se utiliza principalmente para elaborar combustibles, disolventes y anticongelantes. El metanol se puede obtener industrialmente a partir de y , mediante el proceso químico siguiente:
Considerando las reacciones químicas siguientes:
i)
ii)
iii)
Calcula la entalpía de la reacción de obtención del metanol a partir de y .
¿Qué cantidad de energía se cederá o se absorberá para obtener de metanol?
Ejercicio 5 · Opción B
5Opción B
2 puntosContesta solo uno de los dos apartados: 5A o 5B.
El dióxido de azufre () se origina principalmente durante la combustión de combustibles fósiles que contienen azufre, aunque también se puede producir a partir de la descomposición del trióxido de azufre () según la siguiente reacción química ajustada:
Calcula la entalpía de la reacción anterior a .
Si se sabe que el valor de la entropía (), a , para la anterior reacción química es de ; indica, de manera razonada, si esta reacción es espontánea a la temperatura mencionada.
En la ficha de seguridad del compuesto aparece el pictograma siguiente. Indica su significado.