QuímicaAsturiasPAU 2024Ordinaria
Química · Asturias 2024
10 ejercicios
Ejercicio 1
1
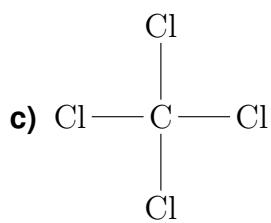
2 puntosRepresente las estructuras de Lewis de las siguientes especies e indique su geometría:

Ejercicio 2
2
2 puntosUtilice un ciclo de Born-Haber para calcular la entalpía estándar de red, , del .
Ejercicio 3
3
2 puntosConsidere la reacción . A una determinada, una mezcla gaseosa de , y se encuentra en un estado de equilibrio. Las cantidades de los tres componentes de la mezcla gaseosa en ese estado de equilibrio se muestran a continuación. La presión de la mezcla gaseosa en dicho estado es .
Calcule el valor de .
Manteniendo la mezcla gaseosa a y , se añaden de . Calcule, en esta nueva situación, el valor del cociente de reacción, .
Compare los valores de y para predecir hacia dónde se desplazará la reacción.
Ejercicio 4
4
2 puntosa) Calcule, a , la entalpía estándar de reacción, , correspondiente a la combustión del metano. b) Indique, razonadamente, si la reacción es exotérmica o endotérmica.
Calcule, a , la entalpía estándar de reacción, , correspondiente a la combustión del metano.
Indique, razonadamente, si la reacción es exotérmica o endotérmica.
Ejercicio 5
5
2 puntosCalcule, a , el pH de una disolución acuosa de .
Ejercicio 6
6
2 puntosCalcule la energía de Gibbs estándar de reacción, , a , correspondiente al proceso que ocurre en una celda galvánica que utiliza los sistemas redox y .
Ejercicio 7
7
2 puntosResponda a las siguientes cuestiones sobre estructura atómica y enlace:
En la tabla aparecen cuatro posibles espín-orbitales descritos por sus correspondientes números cuánticos. Indique, razonadamente, cuál de ellos puede corresponderse con un electrón de la capa de valencia del átomo de azufre en su estado fundamental.
| n | l | ml | ms | |
| 1 | 3 | 2 | 2 | +1/2 |
| 2 | 3 | 1 | 1 | +1/2 |
| 3 | 2 | 1 | 0 | +1/2 |
| 4 | 3 | 2 | 0 | -1/2 |
Indique el tipo de enlace químico que existe en las siguientes sustancias: fluoruro de litio (LiF), hierro (Fe) y diamante (C).
Escriba la fórmula estructural desarrollada de los siguientes compuestos: 3-bromociclohex-1-eno, 2-metilpentano y but-3-en-1-ol.
Ejercicio 8
8
2 puntosEscriba las configuraciones electrónicas de los átomos de flúor, magnesio, fósforo y cromo () en su estado fundamental.
Responda a las siguientes cuestiones sobre reactividad orgánica:
¿Qué nombre recibe el compuesto que se forma al hacer reaccionar propan-2-ol con ácido sulfúrico () concentrado a alta temperatura?
Escriba la fórmula estructural desarrollada de dicho compuesto.
¿Qué tipo de reacción ha tenido lugar?
Ejercicio 9
9
2 puntosLa dependencia de las constantes cinéticas con la temperatura, en reacciones elementales, puede representarse mediante la ecuación de Arrhenius.
Escriba la expresión matemática de la ecuación de Arrhenius.
Explique cómo afecta un incremento de la temperatura a la constante cinética.
Explique cómo afecta la presencia de un catalizador a la constante cinética.
Se muestra, a continuación, la fórmula estructural desarrollada del ibuprofeno.
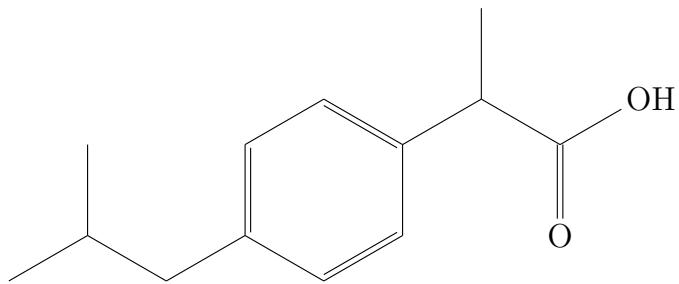
Escriba su fórmula molecular.
Copie en el pliego en blanco la fórmula del compuesto y señale todos los átomos de carbono asimétricos.
Ejercicio 10
10
2 puntosEn la gráfica se muestran dos curvas de valoración ácido-base: una en trazo continuo y la otra en discontinuo. El agente valorante es, en ambos casos, la misma disolución acuosa de hidróxido de sodio, NaOH. En un caso se valora un ácido débil, y en el otro uno fuerte (los dos de la misma concentración). Las dos curvas coinciden a partir de .
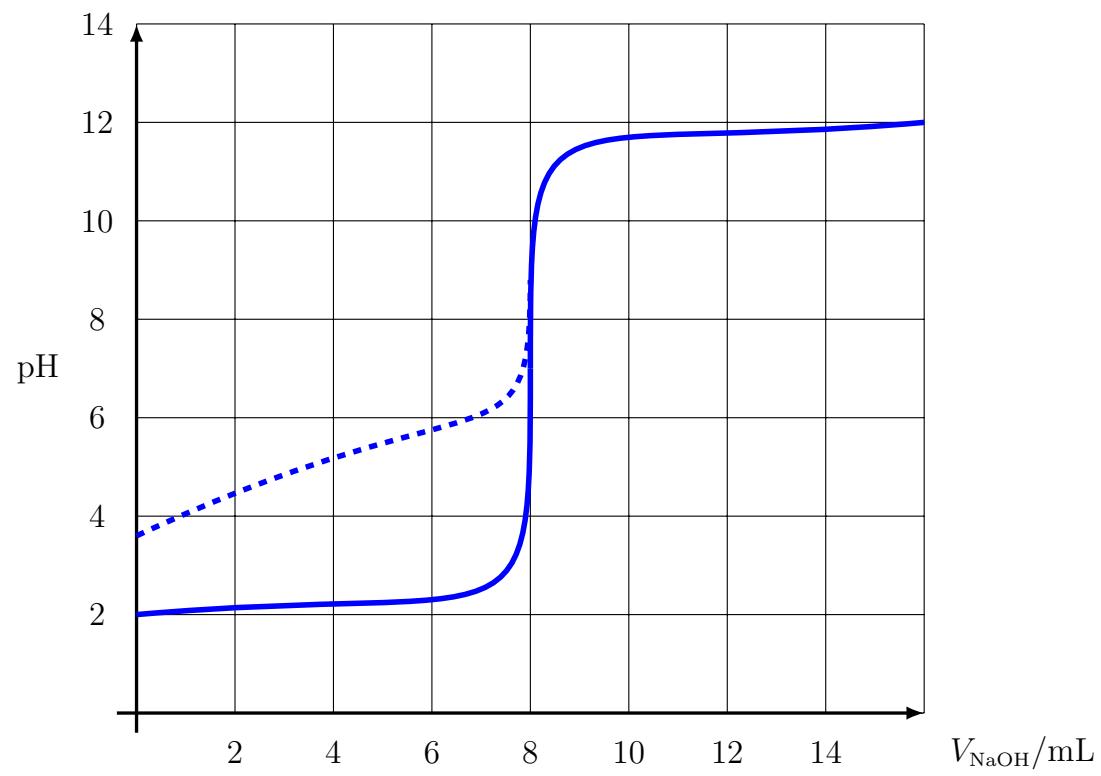
Explique qué curva corresponde a cada ácido.
¿Cuál es el volumen de equivalencia cuando se valora el ácido débil?
¿Cuál es el volumen de equivalencia cuando se valora el ácido fuerte?
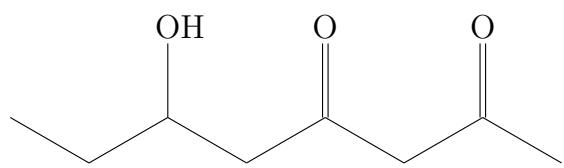
Copie en el pliego en blanco la fórmula estructural desarrollada que se muestra a continuación y señale y nombre todos los grupos funcionales que aparecen en ella.