Determine el orden de reacción de cada reactivo y la constante de velocidad de la reacción.
QuímicaCataluñaPAU 2015Extraordinaria
Química · Cataluña 2015
7 ejercicios
Ejercicio 1
1
2 puntosEl oxígeno y el nitrógeno reaccionan a temperaturas muy elevadas y forman diferentes óxidos de nitrógeno que, una vez liberados a la atmósfera, intervienen en procesos de formación de otros contaminantes. Uno de estos procesos es la oxidación del monóxido de nitrógeno a dióxido de nitrógeno:
La tabla siguiente muestra los datos de un estudio experimental de la cinética de esta reacción, a :
| Experimento | [NO] inicial (mol L-1) | [O2] inicial (mol L-1) | Velocidad inicial (mol L-1s-1) |
| 1 | |||
| 2 | |||
| 3 | |||
| 4 | |||
| 5 |
Realice una representación gráfica aproximada que muestre la energía en función de la coordenada de reacción, suponiendo que la reacción de oxidación del monóxido de nitrógeno se produce en una sola etapa, y señale en ella la energía de activación y la variación de entalpía de la reacción. Si añadimos un catalizador para acelerar la reacción, ¿modificaríamos el valor de la energía de activación? ¿Y el valor de la variación de entalpía de la reacción? Justifique las respuestas.
Ejercicio 2
2
2 puntosEn la fermentación acética del vino, por acción de las bacterias del género Acetobacter, el etanol reacciona con el oxígeno del aire y se transforma en ácido etanoico (llamado habitualmente ácido acético) y agua, mezcla líquida que da lugar al vinagre.
Escriba la reacción de fermentación acética del vino. Calcule su variación de entalpía, en condiciones estándar y a , y justifique si la reacción es endotérmica o exotérmica.
Calcule la variación de energía libre de la reacción de fermentación acética del vino, en condiciones estándar y a , y justifique si la reacción es espontánea.
Ejercicio 3
3
2 puntosLa figura siguiente representa el diagrama de fases del :
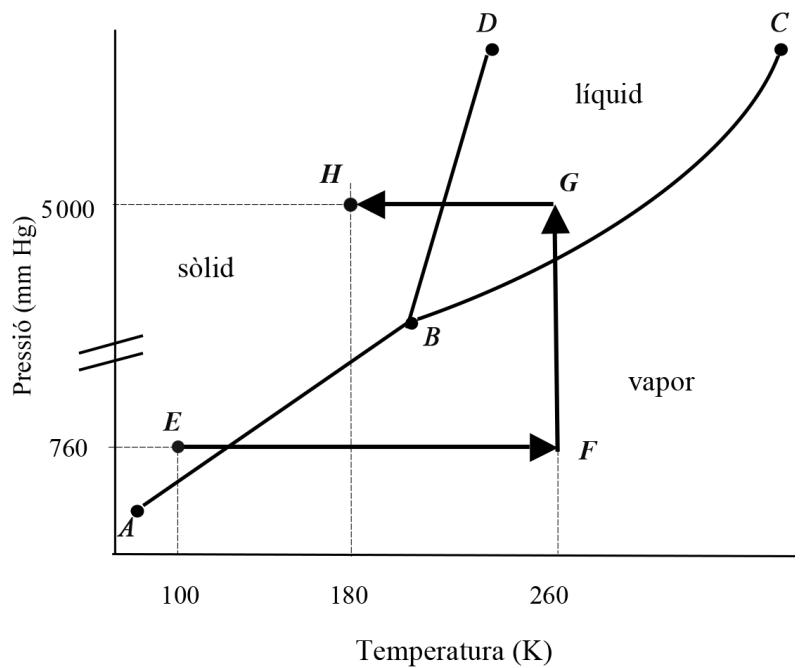
¿Cómo se denominan los puntos B y C? Explique qué representan las líneas AB, BC, BD y el punto B.
Transformamos el dióxido de carbono desde el punto E hasta el punto H, siguiendo las líneas EF-FG-GH. Describa los tres procesos y nombre todos los cambios de fase que se producen.
Ejercicio 4
4
2 puntosElija UNA cuestión entre la 4 y la 5.
Suponga que cuando está a punto de comenzar el partido de la final del Mundial de fútbol de 2018 se descubre que unos ladrones han robado el trofeo, que está hecho de oro. Como no hay tiempo de fabricar uno nuevo para entregarlo al equipo ganador del partido, se decide tomar una reproducción hecha de un metal corriente y recubrirla de una capa fina de oro mediante electrólisis.
Realice un dibujo del montaje experimental que propondría para recubrir la reproducción del trofeo de una capa de oro, si dispusiera de una celda electrolítica, de una solución acuosa de y de un electrodo inerte. ¿Cómo se llama el electrodo donde colocaríamos la reproducción del trofeo y qué polaridad tiene? Escriba la semirreacción que hace que el oro se deposite sobre la reproducción del trofeo.
Si la masa de oro que queremos depositar sobre el trofeo es de , ¿qué intensidad mínima debe tener la corriente eléctrica para que podamos tener dorada la réplica del trofeo antes del final del partido?
Ejercicio 5
5
2 puntosElija UNA cuestión entre la 4 y la 5.
Para mantener las piscinas en condiciones aceptables para el baño se utilizan diferentes productos químicos. Así, para eliminar la materia orgánica y los agentes patógenos se puede utilizar y para controlar el crecimiento de las algas se utilizan sales solubles de cobre(II), como el .
Llenamos una piscina con de agua. ¿Cuál sería el pH del agua de la piscina si añadiéramos de ? Suponga que el agua era inicialmente neutra y que el volumen del agua se mantiene al añadir la sal.
El pH de otra piscina es , valor recomendado normalmente para tener una buena eficiencia en el uso de los productos que añadimos para mantener el agua limpia y libre de microorganismos. ¿Qué concentración máxima de iones puede haber en esta piscina si queremos evitar que se produzca la precipitación del al añadir una sal soluble de cobre(II)?
Ejercicio 6
6
2 puntosElija UNA cuestión entre la 6 y la 7.
El monóxido de nitrógeno es un contaminante que se genera, a veces, como subproducto en un reactor químico. Una manera de eliminarlo consiste en hacerlo reaccionar con hidrógeno según la ecuación siguiente:
Introducimos de monóxido de nitrógeno y de hidrógeno en un recipiente de y lo calentamos hasta una temperatura de . Cuando la reacción alcanza el equilibrio, comprobamos que la mezcla contiene de nitrógeno, además de monóxido de nitrógeno, hidrógeno y agua. Calcule las concentraciones de los cuatro gases en el equilibrio y la constante de equilibrio en concentraciones, , a .
El objetivo de una empresa química es eliminar el monóxido de nitrógeno producido en un reactor mediante la reacción descrita con hidrógeno. ¿Es mejor que realice esta reacción a temperatura alta o baja? ¿Es mejor que la realice a presión alta o baja? Justifique las respuestas.
Ejercicio 7
7
2 puntosElija UNA cuestión entre la 6 y la 7.
El uso tan extendido de combustibles en nuestra sociedad debido a los transportes provoca el vertido de gases a la atmósfera. Así, en la combustión de la gasolina en los motores de los automóviles se produce la emisión de diversos gases, como el monóxido de carbono, el dióxido de carbono y el agua.
Estos gases, al salir del tubo de escape, se difunden a través del aire. Ordene los tres gases mencionados en orden creciente de su velocidad de difusión. Justifique la respuesta.
Hemos comprobado experimentalmente que de dióxido de carbono ocupan a y a . ¿Qué volumen ocuparía esta masa de dióxido de carbono, en las mismas condiciones de presión y de temperatura, si se comportara como un gas ideal? Justifique la diferencia de volúmenes a partir del modelo cinético-molecular de los gases. Indique en qué condiciones de presión y de temperatura el comportamiento de los gases reales es muy parecido al de los gases ideales.
