Escribid la reacción de síntesis del yoduro de hidrógeno a partir de hidrógeno y yodo. Calculad la constante de equilibrio en concentraciones, , de esta reacción a .
QuímicaCataluñaPAU 2014Extraordinaria
Química · Cataluña 2014
7 ejercicios
Ejercicio 1
1
2 puntosEl yoduro de hidrógeno gaseoso es un compuesto muy utilizado en química porque es una de las principales fuentes de yodo. En una industria química hemos introducido moles de y moles de en un reactor de L, y lo calentamos a ; cuando la mezcla alcanza el equilibrio comprobamos que hemos obtenido moles de yoduro de hidrógeno gaseoso.
¿Qué efecto tendrá la adición de más yodo o de un catalizador en la constante de equilibrio en concentraciones, ? ¿Qué efecto tendrá la adición de más yodo o de un catalizador en el rendimiento de la reacción? Argumentad las respuestas, suponiendo que siempre mantenemos la temperatura a .
Ejercicio 2
2
2 puntosEn el laboratorio disponemos de tres vasos de precipitados (A, B y C) que contienen mL de soluciones acuosas de la misma concentración, a una temperatura de . Uno de los vasos contiene una solución de ; otro contiene una solución de , y el otro, una solución de (ácido débil llamado habitualmente ácido propiónico). Medimos el pH de las tres soluciones y obtenemos los resultados siguientes:
| Vaso de precipitados | A | B | C |
| pH medido | 7,0 | 1,5 | 4,0 |
Identificad el contenido de cada vaso y justificad la respuesta.
Si añadimos mL de agua destilada a cada vaso y mantenemos la temperatura a , ¿aumentará, disminuirá o se mantendrá el pH en cada uno de los vasos? Explicad razonadamente la respuesta.
Ejercicio 3
3
2 puntosEn los vuelos espaciales, la masa de combustible es mucho más importante que el volumen que ocupa porque cuanto mayor es la masa más cuesta escapar del campo gravitatorio terrestre. La hidrazina () ha sido utilizada como combustible para los cohetes porque su reacción con el agua oxigenada es muy exotérmica:
Calculad la cantidad de energía producida en forma de calor, a presión constante, en la reacción de un kilogramo de hidrazina con un kilogramo de agua oxigenada, en condiciones estándar y a .
Calculad la energía de enlace , en condiciones estándar y a .
Ejercicio 4 · Opción A
4Opción A
2 puntosElija entre la cuestión 4 y la 5.
Queremos montar una pila, en condiciones estándar y a , que tiene la notación siguiente:
Escribid las semirreacciones que se producen en el ánodo y en el cátodo e indicad su polaridad. Escribid la reacción global de la pila y calculad su fuerza electromotriz.
Explicad el procedimiento experimental para construir esta pila en el laboratorio y medir su fuerza electromotriz. Indicad, también, el material y los reactivos que necesitáis.
Ejercicio 5 · Opción B
5Opción B
2 puntosElija entre la cuestión 4 y la 5.
Tanto el ion potasio como el ion hidrogenotartrato están presentes de manera natural en los vinos y, por este motivo, el equilibrio de solubilidad del hidrogenotartrato de potasio tiene un papel importante en las propiedades del vino, ya que puede dar lugar a vinos turbios.
Si la concentración de ion potasio en un vino es , ¿cuál debería ser la concentración máxima de ion hidrogenotartrato en este vino, a , para que no precipite hidrogenotartrato de potasio? Expresad el resultado en .
El ion hidrogenotartrato es una especie que proviene del ácido tartárico según la reacción siguiente:
Si consideramos solo esta reacción, y sabemos que un vino contiene en equilibrio de ácido tartárico y de ion hidrogenotartrato, ¿cuál es el pH del vino a ?
Ejercicio 6 · Opción A
6Opción A
2 puntosElija entre la cuestión 6 y la 7.
Un laboratorio ha estudiado la cinética de la reacción de oxidación de talio(I) con cerio(IV) en presencia de manganeso(II) como catalizador, en solución acuosa y a la temperatura de . Los resultados experimentales obtenidos avalan el mecanismo de reacción siguiente en tres etapas:
Etapa 1:
Etapa 2:
Etapa 3:
Escribid la reacción global. Explicad qué es un catalizador y cómo interviene en la cinética de una reacción empleando un modelo cinético.
Dado que la etapa 1 del mecanismo es la más lenta de las tres, la velocidad de la reacción global es de orden 1 respecto del y de orden 1 respecto del . Escribid la ecuación de velocidad de la reacción global y justificad en qué unidades se expresa la velocidad de reacción y en qué unidades se expresa la constante de velocidad de esta reacción.
Ejercicio 7 · Opción B
7Opción B
2 puntosElija entre la cuestión 6 y la 7.
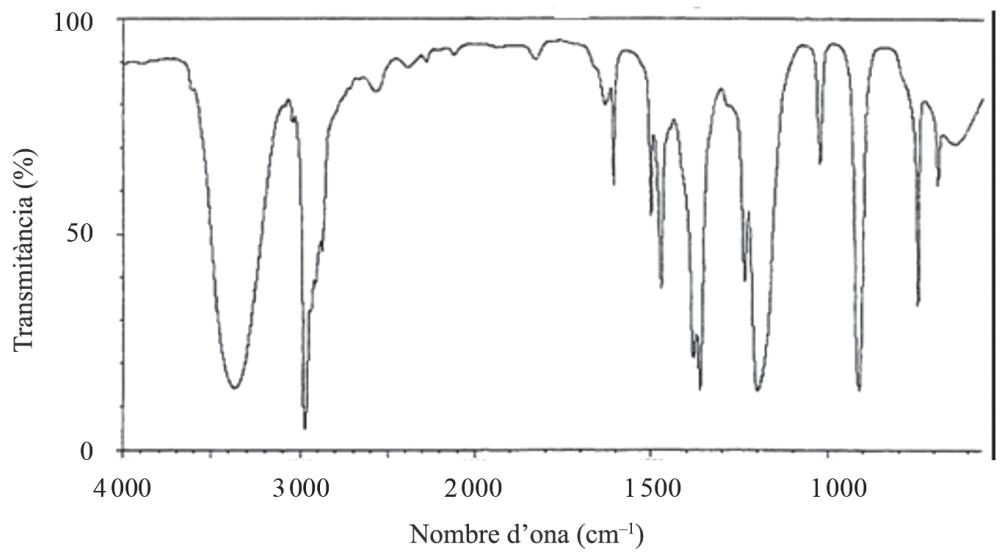
Una industria química ha utilizado la espectroscopia de infrarrojo (IR) para identificar un compuesto puro. Experimentalmente se ha obtenido el espectro siguiente:
| Enlace | Tipo de compuesto | Intervalo de número de onda (cm-1) |
| C-H | alcanos (C-C-H) | 2 850-2 970 |
| 1 340-1 470 | ||
| alquenos (C=C-H) | 3 010-3 095 | |
| 675-995 | ||
| O-H | alcoholes | 3 200-3 600 |
| ácidos carboxílicos | 2 500-2 700 | |
| C-O | alcoholes, éteres, ácidos carboxílicos, ésteres | 1 050-1 300 |
| C=O | aldehídos, cetonas, ácidos carboxílicos, ésteres | 1 690-1 760 |
¿Qué le pasa a una molécula cuando absorbe radiación infrarroja? Justificad si el compuesto puro es el 2-propanol o el ácido propanoico.
La zona de a de un espectro IR se denomina huella dactilar y es característica de cada compuesto. En el espectro obtenido observamos un pico intenso a en esta zona. Calculad la longitud de onda, la frecuencia y la energía de este pico.
