Calcule la constante de equilibrio en concentraciones, , y la constante de equilibrio en presiones, , de la reacción anterior a .
QuímicaCataluñaPAU 2015Ordinaria
Química · Cataluña 2015
14 ejercicios90 min de duración
Ejercicio 1 · Sèrie 2
1Sèrie 2
2 puntosEl dióxido de nitrógeno es un gas contaminante de las zonas urbanas que se forma como subproducto en los procesos de combustión a temperaturas elevadas. En un reactor cerrado de de capacidad calentamos una muestra de dióxido de nitrógeno hasta una temperatura constante de y se produce la reacción siguiente:
Una vez llegamos al equilibrio, analizamos la mezcla gaseosa y encontramos que contiene de , de y de .
¿Conseguiríamos producir más monóxido de nitrógeno si añadimos un catalizador a la mezcla gaseosa en equilibrio? ¿Y si aumentamos el volumen del recipiente? Explique razonadamente las respuestas.
Ejercicio 1 · Sèrie 4
1Sèrie 4
2 puntosSerie 4
Con el paso del tiempo, las tuberías pueden tener problemas de obturación debido a residuos que pueden quedar adheridos. En el mercado encontramos diferentes desatascadores comerciales líquidos, algunos de los cuales son a base de . Para determinar la concentración de este compuesto en el producto comercial podemos efectuar una valoración ácido-base empleando como valorante una solución de ácido clorhídrico de concentración conocida.

Valoramos de un desatascador comercial líquido que contiene con una solución de ácido clorhídrico y se requieren de esta solución ácida para llegar al punto final. Escriba la reacción de valoración y calcule la concentración de que contiene el desatascador comercial líquido, expresada en .
Explique el procedimiento experimental que seguiría en el laboratorio para llevar a cabo esta valoración e indique el material y los reactivos que utilizaría.
Ejercicio 2 · Sèrie 2
2Sèrie 2
2 puntosQueremos fabricar pilas de diferente fuerza electromotriz en el laboratorio y disponemos de electrodos de los metales siguientes: cobre, níquel y hierro. Preparamos soluciones de concentración de los iones , y a partir de sales solubles en agua y, además, disponemos de una solución acuosa concentrada de .
De todas las pilas que podemos montar, justifique cuál tendrá la fuerza electromotriz máxima. Calcule dicha fuerza electromotriz.
Explique cómo montaría en el laboratorio una pila en la que los electrodos fuesen el níquel y el hierro, y mencione el material y los reactivos necesarios. Dibuje un esquema de la pila e indique la polaridad de los electrodos.
Ejercicio 2 · Sèrie 4
2Sèrie 4
2 puntosSerie 4
La nitroglicerina, , que tradicionalmente se ha utilizado para fabricar explosivos, también se usa en medicina como vasodilatador para tratar la angina de pecho. Podemos representar la descomposición de la nitroglicerina mediante la ecuación siguiente:
Una dosis de nitroglicerina para tratar la angina de pecho es de . Si suponemos que esta cantidad se acaba descomponiendo totalmente en el organismo según la reacción química anterior, calcule qué volumen de oxígeno obtendríamos, medido a y a , y qué cantidad de calor se liberaría a presión constante, en condiciones estándar y a .
Calcule la entalpía estándar de formación de la nitroglicerina a .
Ejercicio 3 · Sèrie 2
3Sèrie 2
2 puntosObserve el gráfico siguiente que muestra el radio atómico de los elementos de la tabla periódica. A partir de las configuraciones electrónicas de los átomos o iones, y utilizando el modelo atómico de cargas eléctricas, responda a las cuestiones siguientes:
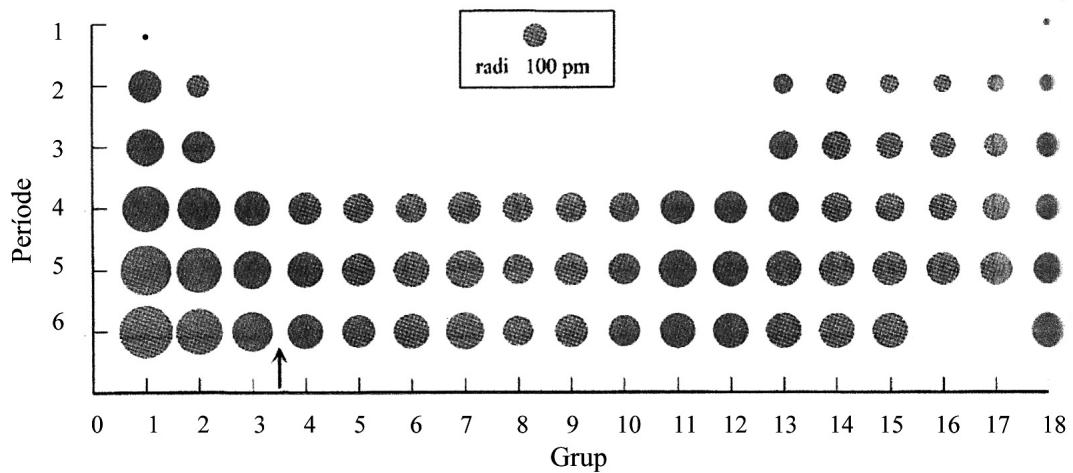
Explique la diferencia de radio atómico entre el átomo de berilio y el de estroncio. Justifique cuál de estos dos elementos tiene la primera energía de ionización más grande.
El cloruro de potasio es un compuesto iónico que contiene los iones y en la red cristalina. Explique razonadamente si el radio del catión es más grande o más pequeño que el radio del átomo de , y si el radio del anión es más grande o más pequeño que el radio del átomo de .
Ejercicio 3 · Sèrie 4
3Sèrie 4
2 puntosSerie 4
Los propulsores iónicos son un tipo de propulsores de naves espaciales que utilizan un haz de iones positivos acelerados a velocidades muy elevadas. La propulsión iónica inicialmente utilizaba cesio, pero, por problemas de erosión de los materiales, actualmente se emplean gases nobles como el xenón.

Cuando hacemos incidir sobre átomos de xenón una radiación electromagnética con una longitud de onda máxima de , se provoca la formación del catión . ¿Cuál es la frecuencia de esta radiación electromagnética? ¿Qué valor tiene la primera energía de ionización del xenón, expresado en ?
Escriba la configuración electrónica, en estado fundamental, de los átomos de cesio y de xenón. A partir de las configuraciones electrónicas y del modelo atómico de cargas eléctricas, compare el radio atómico y la primera energía de ionización del cesio y del xenón.
Ejercicio 4 · Sèrie 2
4Sèrie 2
2 puntosElija UNA cuestión entre la 4 y la 5.
El ácido acetilsalicílico , principio activo de la aspirina, es un ácido débil y monoprótico, ya que en la fórmula química tiene un único grupo ácido . Preparamos una solución de ácido acetilsalicílico en agua de concentración , y el pH medido es de a la temperatura de .

Calcule la constante de acidez, , del ácido acetilsalicílico a .
Valoramos de otra solución de ácido acetilsalicílico con hidróxido de sodio y gastamos de esta base para llegar al punto final. Escriba la reacción de valoración y calcule la concentración de la solución de ácido acetilsalicílico, expresada en .
Ejercicio 4 · Sèrie 4
4Sèrie 4
2 puntosSerie 4
Elija UNA cuestión entre la 4 y la 5.
El monóxido de nitrógeno es el producto de la reacción entre el nitrógeno y el oxígeno atmosféricos que tiene lugar en los coches, dadas las temperaturas elevadas que se alcanzan. Este óxido se libera a la atmósfera y rápidamente se oxida a dióxido de nitrógeno, según el proceso siguiente:
Realizamos un experimento en un recipiente cerrado, a volumen constante y a la temperatura de , introduciendo , y hasta que la presión parcial de cada gas es , y , respectivamente. Justifique, a partir de los cálculos necesarios, por qué la reacción química no está en equilibrio. ¿La presión parcial del será más alta o más baja cuando la reacción alcance el equilibrio? Justifique la respuesta.
Determinamos la constante de equilibrio en presiones, , de la reacción anterior para diferentes temperaturas y obtenemos los datos de la tabla. ¿La reacción de oxidación del a es exotérmica o endotérmica? Para favorecer la oxidación del a , a una temperatura determinada, ¿es preferible realizar el experimento en un reactor cerrado de o de ? Justifique las respuestas.
| Temperatura (K) | 600 | 700 | 800 | 900 | 1000 |
| Constante de equilibrio (Kp) | 138 | 5,12 | 0,436 | 0,0626 | 0,0130 |
Ejercicio 5 · Sèrie 2
5Sèrie 2
2 puntosElija UNA cuestión entre la 4 y la 5.
La glucosa es un monosacárido muy presente en nuestra vida, ya que las células lo utilizan como fuente de energía y como intermediario metabólico. Una de las reacciones que se pueden producir en nuestro organismo es la siguiente:
A partir de los datos termodinámicos de la tabla, calcule qué cantidad de energía en forma de calor proporciona al organismo la reacción de un mol de glucosa para formar etanol, si se produce a presión constante.
| Compuesto | |||
| Entalpía estándar de formación, a () |
Justifique si la cantidad de energía en forma de calor que proporciona al organismo la reacción de un mol de glucosa para formar etanol, a volumen constante, sería igual, superior o inferior a la que proporcionaría la reacción si se efectuase a presión constante.
Ejercicio 5 · Sèrie 4
5Sèrie 4
2 puntosSerie 4
Elija UNA cuestión entre la 4 y la 5.
Las baterías recargables de ion litio se utilizan en los dispositivos móviles y en los ordenadores. Contienen un electrodo formado por los materiales y , y otro electrodo formado por los materiales y . La batería tiene, además, una sustancia entre los electrodos para facilitar el movimiento de los iones .
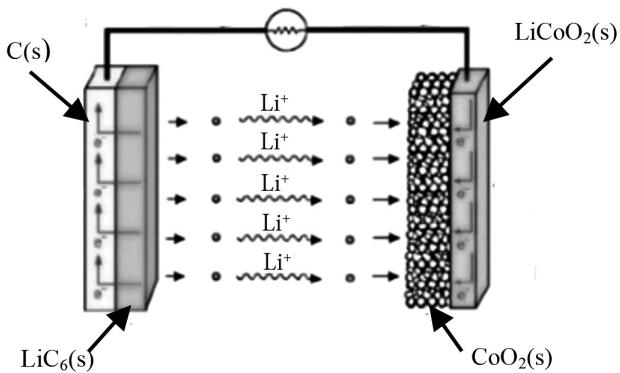
Cuando esta batería funciona como una pila, las semirreacciones que se producen en los electrodos son las indicadas. Justifique qué semirreacción se produce en el ánodo y cuál se produce en el cátodo, y escriba la reacción global. Calcule la fuerza electromotriz de la batería si sabemos que la variación de energía libre de la reacción global es por mol de .
Cuando cargamos la batería, efectuamos un proceso electrolítico y regeneramos y en los electrodos, según las semirreacciones indicadas. Calcule la masa de que se formará en uno de los electrodos si cargamos la batería durante y hacemos pasar una intensidad de corriente de .
Ejercicio 6 · Sèrie 2
6Sèrie 2
2 puntosElija UNA cuestión entre la 6 y la 7.
El cloruro de nitrosilo (), compuesto que se utiliza en síntesis química para introducir grupos en diversas moléculas orgánicas, se puede formar a partir de la reacción siguiente:
Hemos estudiado la influencia de la concentración de los reactivos en la velocidad de esta reacción a una temperatura determinada y hemos obtenido los resultados siguientes:
| Concentración inicial de () | Concentración inicial de () | Velocidad inicial de la reacción () |
Justifique el orden de la reacción respecto a cada reactivo y calcule la constante de velocidad.
Explique en qué se basa el modelo cinético de colisiones. Justifique a partir de este modelo cinético el efecto de la temperatura y del volumen del reactor en la velocidad de la reacción.
Ejercicio 6 · Sèrie 4
6Sèrie 4
2 puntosSerie 4
Elija UNA cuestión entre la 6 y la 7.
El fluoruro de nitrilo () es un gas incoloro que se utiliza como agente para la fluoración y lo podemos sintetizar a partir de dióxido de nitrógeno y flúor gaseosos. El mecanismo de esta reacción de síntesis se produce en dos etapas elementales:
Etapa 1 (lenta):
Etapa 2 (rápida):
Escriba la reacción global de la síntesis del fluoruro de nitrilo. Justifique el orden de la reacción de la etapa 1 respecto de cada uno de los reactivos y escriba la ecuación de velocidad de la reacción de la etapa 1. Indique en qué unidades se expresa la velocidad de una reacción química.
Empleando el modelo de colisiones o el modelo del estado de transición (o complejo activado), explique el concepto energía de activación y la influencia de la temperatura en la velocidad de una reacción química.
Ejercicio 7 · Sèrie 2
7Sèrie 2
2 puntosElija UNA cuestión entre la 6 y la 7.
El bromo, , es una sustancia rojiza y líquida a y . A partir del diagrama de fases del bromo podemos extraer los datos siguientes:
| Punto de fusión | Punto triple | Punto crítico |
¿Qué información nos dan el punto de fusión y el punto triple del bromo? Explique razonadamente qué observaremos si en un recipiente cerrado que contiene bromo, a y , vamos disminuyendo la presión mientras mantenemos la temperatura.
Podemos representar el proceso de transformación del bromo líquido en bromo gaseoso mediante la ecuación química siguiente:
Determine, expresada en , la temperatura de ebullición del bromo a , suponiendo que las variaciones de entalpía y de entropía estándar de este compuesto no cambian con la temperatura.
Ejercicio 7 · Sèrie 4
7Sèrie 4
2 puntosSerie 4
Elija UNA cuestión entre la 6 y la 7.
Los detergentes contienen grandes cantidades de fosfatos, que son una de las causas de contaminación de las aguas. El saneamiento es un proceso clave para garantizar la calidad del agua y, por tanto, la salud y la preservación del medio. Un método para eliminar los fosfatos de las aguas residuales consiste en precipitarlos como fosfato de aluminio, .
Escriba la reacción del equilibrio de solubilidad del fosfato de aluminio. Calcule la solubilidad de esta sal a , expresada en .
Se quiere verter un agua residual con una concentración muy alta de fosfatos en un acuífero donde, por exigencias legales, solo está permitido verter agua con una concentración de fosfatos menor de . Por ello, antes de verterla se añade una cantidad de que consigue precipitar una parte del fosfato y deja una concentración en equilibrio del ion en el agua de . Justifique si el agua residual tratada cumple las exigencias legales para verterla al acuífero. Suponga que la temperatura del agua es de .
