El premio Nobel de Química del año 2017 fue concedido a los investigadores Jacques Dubochet, Joachim Frank y Richard Henderson (figura 1) por el desarrollo de nuevas técnicas que permiten la observación y la determinación estructural de biomoléculas en alta resolución. Un ejemplo de biomolécula es la vainillina (figura 2).

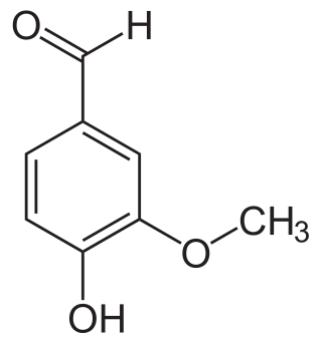
Determina el peso molecular de la vainillina.
Indica dos grupos funcionales presentes en la vainillina.