Escriba la reacción de transformación de la cal viva en cal apagada y explique razonadamente si la reacción absorbe o desprende calor, en condiciones estándar y a , cuando se lleva a cabo a presión constante.
QuímicaCataluñaPAU 2013Ordinaria
Química · Cataluña 2013
14 ejercicios
Ejercicio 1 · Sèrie 3
1Sèrie 3
2 puntosSèrie 3Serie 3
La cal viva, , se utiliza en el tratamiento de aguas y en la eliminación del dióxido de azufre de los gases de las chimeneas de las centrales térmicas, mientras que la cal muerta o apagada, , se usa junto con arena y agua en los morteros empleados en la construcción para unir ladrillos. Si ponemos agua en contacto con la cal viva, esta se hidrata y origina la cal apagada. Observe la tabla siguiente y responda a las cuestiones:
| Sustancia | \( \Delta H_f^\circ (\text{kJ mol}^{-1}) \) | \( \Delta G_f^\circ (\text{kJ mol}^{-1}) \) |
| CaO(s) | -635,1 | -604,0 |
| \( \text{Ca(OH)}_2(\text{s}) \) | -985,8 | -898,5 |
| \( \text{H}_2\text{O}(\text{l}) \) | -285,8 | -237,1 |
Explique razonadamente si la reacción de transformación de la cal viva en cal apagada es espontánea, en condiciones estándar y a .
Ejercicio 1 · Sèrie 4
1Sèrie 4
2 puntosEl eteno, hidrocarburo insaturado llamado habitualmente etileno, es uno de los compuestos químicos orgánicos producidos en más cantidad en el mundo. La principal aplicación que tiene es la fabricación del polímero polietileno, empleado para la elaboración de bolsas de plástico. También se puede transformar en etano mediante reacciones de adición de hidrógeno en presencia de catalizadores, como, por ejemplo, el paladio:
Calcule la entalpía estándar de esta reacción, a , empleando los valores de la tabla siguiente:
| Enlace | C-H | C-C | C=C | H-H |
| Entalpía de enlace, en condiciones estándar y a 298 K (en kJ mol-1) | 413 | 348 | 614 | 436 |
Explique razonadamente si la variación de entropía de esta reacción () es positiva o negativa, y también si la reacción será espontánea a temperaturas altas o bajas.
Ejercicio 2 · Sèrie 3
2Sèrie 3
2 puntosSèrie 3Serie 3
La formamida, , es un compuesto orgánico de gran importancia en la obtención de fármacos y fertilizantes. A altas temperaturas, la formamida se disocia en amoníaco y monóxido de carbono de acuerdo con el equilibrio según:
En un recipiente industrial de , en el cual previamente se ha hecho el vacío y se ha mantenido una temperatura de , se añade formamida hasta que la presión inicial en el interior es de .
Calcule la concentración de formamida que contiene el recipiente una vez se ha alcanzado el equilibrio, expresada en .
Explique razonadamente cómo variará la concentración de formamida si a la mezcla en equilibrio se le añade un poco de amoníaco. ¿Y si aumentamos el volumen del recipiente?
Ejercicio 2 · Sèrie 4
2Sèrie 4
2 puntosUn estudiante lleva a cabo el experimento siguiente en el laboratorio, a una temperatura de : transfiere a un vaso de precipitados, con la ayuda de una probeta, de una solución acuosa de , y de una solución acuosa de . Remueve bien la mezcla con una varilla de vidrio y observa enseguida la aparición de un precipitado de color blanco.
Explique razonadamente, a partir de los cálculos necesarios, la formación del precipitado.
El estudiante separa el precipitado blanco de la solución acuosa incolora mediante un proceso de filtración. Con la solución acuosa del filtrado llena dos tubos de ensayo hasta la mitad; en uno añade un poco de una solución acuosa concentrada de y en el otro, un poco de agua destilada. Explique razonadamente qué sucederá en cada tubo.
Ejercicio 3 · Sèrie 3
3Sèrie 3
2 puntosSèrie 3Serie 3
Uno de los problemas principales de las cafeteras son los depósitos de cal que se generan porque las estropean y alteran el sabor del café. Por este motivo es conveniente descalcificarlas periódicamente y se recomienda utilizar descalcificadores a base de ácido láctico, el cual, además de ser eficaz contra la cal, es biodegradable y no corrosivo para las piezas metálicas de la cafetera. La etiqueta de la botella de un descalcificador comercial líquido dice que contiene un en masa de ácido láctico. Para determinar la concentración exacta de este ácido se quiere hacer una volumetría ácido-base en el laboratorio.

Dado que el descalcificador comercial es demasiado concentrado para valorarlo directamente, decidimos diluirlo diez veces con agua destilada, de manera que la concentración de ácido láctico en la solución diluida será del en masa. Para hacerlo, disponemos de los lotes de material de vidrio siguientes:
<table><tr><td>Lote A</td><td>pipeta aforada de 5 mL<br>probeta de 50 mL</td></tr><tr><td>Lote B</td><td>pipeta aforada de 10 mL<br>matraz aforado de 1 000 mL</td></tr><tr><td>Lote C</td><td>pipeta aforada de 10 mL<br>matraz aforado de 100 mL</td></tr><tr><td>Lote D</td><td>probeta de 10 mL<br>matraz aforado de 100 mL</td></tr></table>
Explique razonadamente cuál de los cuatro lotes permitirá hacer la dilución con más precisión, y justifique la eliminación de los otros tres.
Explique el procedimiento experimental que seguiría en el laboratorio para llevar a cabo la valoración de de la solución diluida del descalcificador con una solución de , e indique el material y los reactivos que utilizaría.
Ejercicio 3 · Sèrie 4
3Sèrie 4
2 puntosEl magnesio es un elemento metálico que forma parte de muchas aleaciones, pero no se encuentra puro en la naturaleza. Se puede obtener a partir de alguna de sus sales empleando una celda electrolítica.
Escriba las semirreacciones que se producen en cada electrodo, y la reacción global cuando se lleva a cabo la electrólisis de cloruro de magnesio fundido, e indique el nombre y la polaridad de los electrodos.
Justifique por qué hay que realizar el proceso de obtención de magnesio en una celda electrolítica y no en una celda galvánica (pila). Si por la celda electrolítica de cloruro de magnesio fundido circula una intensidad de corriente de , ¿cuántas horas deben transcurrir para conseguir de magnesio?
Ejercicio 4 · Sèrie 3
4Sèrie 3
2 puntosSèrie 3Serie 3
Elija UNA cuestión entre la 4 y la 5.
En el diagnóstico de enfermedades respiratorias se utiliza como prueba la difusión pulmonar de monóxido de carbono () que permite evaluar el proceso de transferencia de oxígeno desde los pulmones (alvéolos) hasta la unión con la hemoglobina contenida en los glóbulos rojos de la sangre.
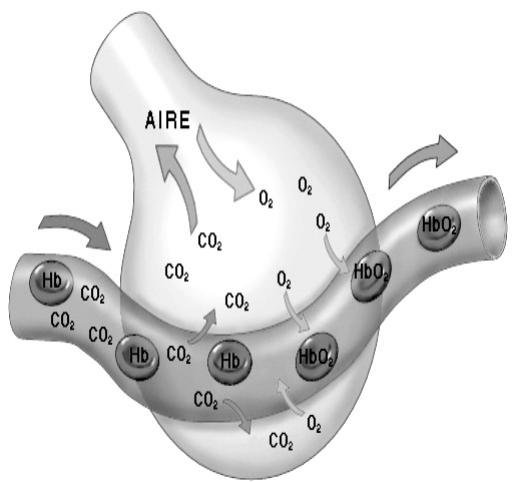
¿En qué consiste la difusión gaseosa? ¿Qué relación hay entre la velocidad de difusión del oxígeno y la del monóxido de carbono?
El volumen molar del es y el del es , a y . Determine el volumen molar de un gas ideal en estas condiciones y justifique la posible desviación del comportamiento ideal de los dos gases a partir de la teoría cinético-molecular de los gases.
Ejercicio 4 · Sèrie 4
4Sèrie 4
2 puntosElija UNA cuestión entre la 4 y la 5.
El salfumán es un producto comercial que contiene y que se utiliza para la limpieza y desinfección de inodoros. Para determinar el contenido de de un salfumán comercial se puede llevar a cabo una valoración ácido-base empleando hidróxido de sodio como reactivo valorante.

Disponemos de una solución de hidróxido de sodio . ¿Qué volumen de esta solución necesitamos para preparar de una solución de hidróxido de sodio ? Indique el material necesario para preparar esta solución en el laboratorio.
Explique el procedimiento experimental para llevar a cabo la valoración de de la muestra de salfumán con la solución de hidróxido de sodio , e indique el material y los reactivos que utilizaría.
Ejercicio 5 · Sèrie 3
5Sèrie 3
2 puntosSèrie 3Serie 3
Elija UNA cuestión entre la 4 y la 5.
El monóxido de nitrógeno se puede reducir a nitrógeno según la reacción siguiente:
Se diseñó un conjunto de experiencias, a , que permitió determinar que la reacción es de orden 2 respecto al monóxido de nitrógeno, que es de orden 1 respecto al hidrógeno, y que el valor de la constante de velocidad es . En un reactor de volumen fijo introducimos la misma cantidad, en moles, de monóxido de nitrógeno y de hidrógeno, y calentamos la mezcla a para que comience la reacción.
Calcule la concentración de hidrógeno en el reactor cuando la concentración de monóxido de nitrógeno es . ¿Cuál es la velocidad de la reacción en este instante?
¿Cómo se ve afectada la velocidad de la reacción si introducimos un catalizador en el reactor? ¿Y si aumentamos la temperatura? Explique razonadamente las respuestas a partir de un modelo cinético.
Ejercicio 5 · Sèrie 4
5Sèrie 4
2 puntosElija UNA cuestión entre la 4 y la 5.
Los gases amoníaco y bromuro de hidrógeno se difunden en un tubo estrecho, en sentidos opuestos, y salen de los puntos X e Y en el mismo instante. Cuando se encuentran, forman bromuro de amonio, .
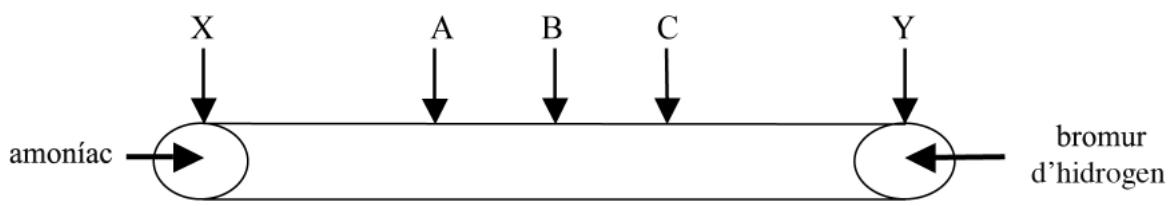
Explique razonadamente si el bromuro de amonio se formará en el punto A, B o C de la figura.
El amoníaco gaseoso tiene una densidad de a y a . Calcule su densidad en estas condiciones de presión y temperatura si se comportara como un gas ideal, y justifique la diferencia a partir del modelo cinético-molecular de los gases.
Ejercicio 6 · Sèrie 3
6Sèrie 3
2 puntosSèrie 3Serie 3
Elija UNA cuestión entre la 6 y la 7.
La presencia de hierro es uno de los problemas que más a menudo deben afrontar los profesionales de tratamiento de aguas. Este elemento puede afectar el sabor del agua, producir manchas en los sanitarios y en la ropa blanca o formar depósitos en las redes de distribución.
Las guías de calidad de la Organización Mundial de la Salud recomiendan que las aguas destinadas al consumo humano no sobrepasen los de hierro. Si suponemos que esta concentración es toda de , ¿qué pH tendrá el agua cuando comience la precipitación del hidróxido de hierro(II)?
En un vaso de precipitados tenemos un poco de hidróxido de hierro(II) sólido en contacto con una solución acuosa saturada de este hidróxido. Una manera de solubilizar el sólido es añadir agua destilada. Explique otras dos maneras de solubilizarlo.
Ejercicio 6 · Sèrie 4
6Sèrie 4
2 puntosElija UNA cuestión entre la 6 y la 7.
La producción de la propanona, , llamada habitualmente acetona, es un indicador de crecimiento económico por el gran uso que se hace de ella en la industria de plásticos, fibras y medicamentos, entre otros productos. Para comprobar la pureza de la acetona producida se pueden emplear técnicas como la espectrometría de masas o la espectrofotometría de infrarrojo. En la figura se muestra el espectro de masas de la acetona:
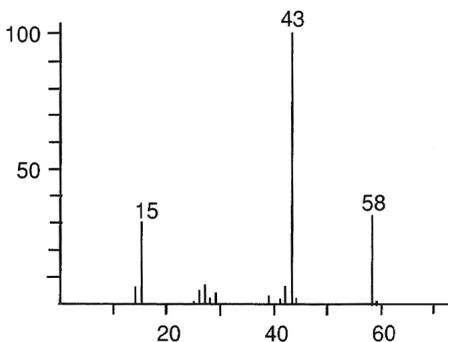
Indique qué magnitud se representa en el eje de abscisas del espectro de masas. Interprete la información del espectro indicando a qué pueden ser debidos los picos que se obtienen en los valores 15, 43 y 58.
¿Qué magnitudes se representan en los dos ejes de un espectre infrarrojo? ¿Qué información útil nos proporcionaría el espectro infrarrojo de una muestra de acetona para comprobar si está o no impurificada con 2-propanol?
Ejercicio 7 · Sèrie 3
7Sèrie 3
2 puntosSèrie 3Serie 3
Elija UNA cuestión entre la 6 y la 7.
Queremos separar la plata de una aleación formada por plata y estaño. Para conseguirlo, podemos escoger entre añadir a la aleación una solución acuosa de ácido sulfúrico o una de ácido nítrico , y, posteriormente, obtener la plata sólida por filtración.
Justifique, desde un punto de vista electroquímico, si elegiría añadir ácido sulfúrico o ácido nítrico.
Escriba la reacción del ácido nítrico en agua, según el modelo ácido-base de Brönsted-Lowry. Si tenemos una solución de ácido nítrico y otra de ácido sulfúrico de la misma concentración molar, ¿cuál de las dos soluciones tiene un pH más alto? Explíquelo razonadamente.
Ejercicio 7 · Sèrie 4
7Sèrie 4
2 puntosElija UNA cuestión entre la 6 y la 7.
El bromo se utiliza en la producción de colorantes, desinfectantes e insecticidas. Una fuente importante para obtenerlo es el agua de mar, donde se encuentra en forma de bromuro. La obtención de bromo a partir del agua de mar se lleva a cabo industrialmente mediante una reacción del tipo:
donde X es otro halógeno.
Explique razonadamente qué halógeno o halógenos pueden hacer que la reacción anterior sea espontánea, y calcule la variación de energía libre estándar, a , de una de estas reacciones.
A partir de la configuración electrónica de los átomos o iones, y utilizando el modelo atómico de cargas eléctricas, compare el radio atómico de los elementos y , así como el radio de las especies químicas y .
