El premio Nobel de Química del año 2022 fue concedido a los investigadores Carolyn R. Bertozzi, Morten Meldal y K. Barry Sharpless (figura 1), por el descubrimiento de nuevas técnicas, como por ejemplo la química del clic, las cuales permiten construir moléculas complejas, utilizadas como fármacos y también como nuevos materiales, a partir de moléculas mucho más sencillas.
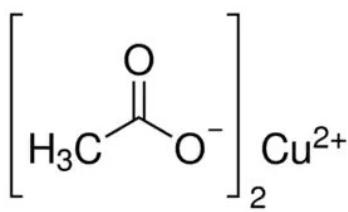
Uno de los reactivos de estructura sencilla utilizados por estos investigadores fue el acetato de cobre (II) (figura 2), el cual se puede obtener a partir del ácido acético o ácido etanoico ().
Para determinar la concentración del ácido acético, en el laboratorio se lleva a cabo una valoración con . Propón, de manera razonada, qué indicador de la siguiente tabla utilizarías para identificar el punto final de la valoración y justifica qué cambio de color observarías.

| Indicador | Intervalo de pH de cambio de color | Cambio de coloración |
| Violeta de metilo | 0,5 - 1,6 | Amarillo-azul |
| Azul de timol | 1,2 - 2,8 | Rojo-amarillo |
| Fenolftaleína | 8,2 - 10,0 | Incoloro-rosa |

