¿Qué elemento tendrá propiedades químicas similares a A?
QuímicaPaís VascoPAU 2014Ordinaria
Química · País Vasco 2014
10 ejercicios90 min de duración
Datos generales del examen
- Masas atómicas (u.m.a.): H: 1
- C: 12
- O: 16
- Cu: 63,5
- Números atómicos (Z): H: 1
- C: 6
- N: 7
- O: 8
- F: 9
- C.N.: Condiciones Normales de presión y temperatura (
- )
- (aq): disolución acuosa
- Condiciones standard:
Ejercicio 1 · A · cuestiones
1A · cuestiones
2 puntosCuestiones
Teniendo en cuenta el fragmento de la tabla periódica de la figura, responder de forma razonada las siguientes preguntas:
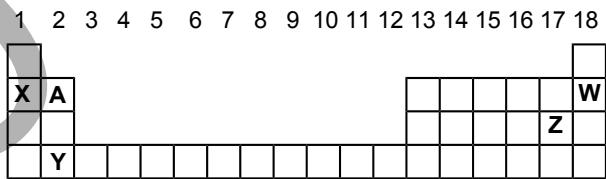
¿Cuál es el elemento de mayor tamaño?
¿Qué elemento tiene más electrones en su última capa?
Comparando los tamaños de los elementos X y W, ¿cuál es mayor?
¿Qué tamaño tendrá el ión respecto de su átomo neutro?
Ejercicio 1 · A · Problemas
1A · Problemas
2,5 puntosLa entalpía de combustión de un compuesto líquido de fórmula es :
Escribe la ecuación termoquímica y calcula cuántos litros de , medidos en C.N., se obtendrán cuando se intercambian . Indicar si la energía se libera o absorbe.
¿Cuántos gramos del compuesto hay que quemar para calentar de agua de a ?
Usando las entalpías de formación del dióxido de carbono y del agua, calcula la entalpía de formación del compuesto y escribe la ecuación termoquímica correspondiente.
Ejercicio 1 · B · cuestiones
1B · cuestiones
2 puntosCuestiones
Para determinar la acidez de un vinagre (porcentaje en masa de ácido acético) se ha empleado . Dada la ecuación:
Calcular la acidez del vinagre sabiendo que se necesitan de para neutralizar de vinagre (densidad del vinagre, ).
En el laboratorio se realiza un montaje como el de la figura para llevar a cabo el proceso.

nombrar cada instrumento y describir cómo se emplea en el proceso.
indicar qué sustancia(s) se coloca(n) en cada elemento del montaje.
indicar los cambios que se observan a lo largo del proceso y cómo se sabe cuándo termina la valoración.
Ejercicio 1 · B · Problemas
1B · Problemas
2,5 puntosDada la siguiente ecuación:
Calcular el cambio de entalpía del proceso y escribir su ecuación termoquímica.
¿Qué cantidad de energía se intercambia al descomponer de agua oxigenada? Indica si dicha energía se libera o absorbe.
Calcular el cambio de entropía del proceso. ¿Es espontáneo en condiciones standard?
¿Cómo será el proceso (espontáneo/forzado) a cualquier otra temperatura?
Ejercicio 2 · A · cuestiones
2A · cuestiones
1,5 puntosCuestiones
Se electroliza una disolución de cloruro de cobre (II) con una corriente de :
Escribir la ecuación química del proceso que ocurre en cada electrodo.
¿Cuántos gramos de cobre metálico se depositan en ?
Tras ese tiempo, ¿cuántos litros de se liberan, medidos en C.N.?
Ejercicio 2 · A · Problemas
2A · Problemas
2,5 puntosLa constante de ionización del ácido HA es
¿Qué concentración tendrá una disolución acuosa del ácido de ? ¿Cuál será la concentración del anión en el equilibrio?
¿De qué concentración deberá ser una disolución de ácido clorhídrico para que ésta tenga un ? ¿Cuál será la concentración de ión cloruro en dicha disolución?
Indica cuál será el pH (ácido, neutro o básico) de las disoluciones acuosas de las sales NaA y NaCl.
Ejercicio 2 · B · cuestiones
2B · cuestiones
1,5 puntosCuestiones
Dada la siguiente ecuación:
Escribir y ajustar la ecuación redox correspondiente.
Indicar las sustancias que se oxidan y reducen en la reacción.
Ejercicio 2 · B · Problemas
2B · Problemas
2,5 puntosA la constante del equilibrio es . En un recipiente de 4 litros se introducen 3 moles de HI:
Calcular la concentración de cada sustancia en el equilibrio.
Calcular la presión parcial del hidrógeno(g) en el equilibrio.
Si el proceso es exotérmico, ¿en qué sentido se desplazará el equilibrio y cómo cambiará el número de moles de HI si:
se aumenta la presión?
se sube la temperatura?
Ejercicio 3 · Opción A
3Opción A
1,5 puntosCuestiones
Nombra y representa las fórmulas semidesarrolladas de:
Tres derivados del ácido propanóico (dos ésteres y una amida).
Un alcohol, un aldehído y una cetona, isómeros entre sí y con 4 átomos de C.
Completa estas ecuaciones, dibuja las fórmulas semidesarrolladas de todas las sustancias y nombra los productos:
Propeno + agua
2-Butanol + oxidante suave
Ejercicio 3 · Opción B
3Opción B
1,5 puntosCuestiones
Dadas las siguientes moléculas: , y
Dibuja sus estructuras de Lewis.
Indica la geometría de cada molécula empleando la teoría de Repulsión de Electrones de Valencia.
¿Qué moléculas tienen momento dipolar no nulo?
