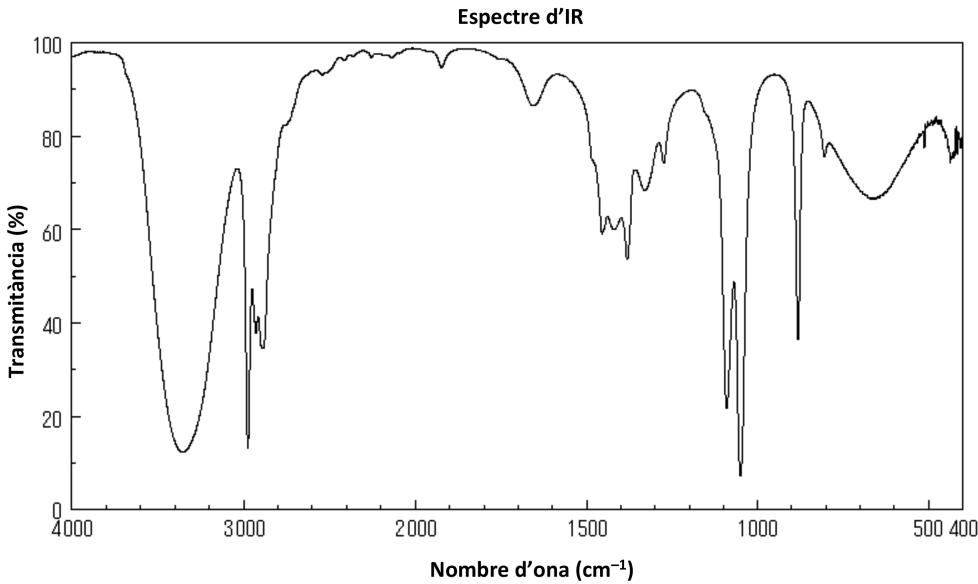
Calculad la entalpía de combustión de de etanol utilizando las energías de enlace. Razonad, después de hacer los cálculos adecuados, cuál de los dos combustibles (etanol o éter dimetílico) resulta más eficiente desde el punto de vista energético por unidad de masa, en condiciones estándar a .
| Enlace | C-C | C-H | C-O | O-H | O=O | C=O |
| Entalpía de enlace a 25 °C y 1 atm (kJ mol-1) | 348 | 412 | 358 | 463 | 498 | 799 |