¿Cuál es la solubilidad molar de las sales de carbonato de calcio y de carbonat de magnesio a ?
Cuando la concentración de carbonato es , ¿a partir de qué concentración de calcio (en ) precipita el carbonato de calcio?
¿A partir de qué concentración de magnesio (en ) precipita el carbonato de magnesio?
QuímicaCataluñaPAU 2020Ordinaria
Química · Cataluña 2020
14 ejercicios
Ejercicio 1 · Opción A
1Opción A
2,5 puntosSèrie 1
La dureza es una cualidad del agua relacionada con el contenido en disolución de cationes alcalinotérreos, principalmente calcio y magnesio. Un efecto de la dureza del agua se observa en las incrustaciones de sales de carbonato que se producen dentro de los depósitos que contienen agua caliente.
¿Cómo se verá afectado el equilibrio de solubilidad de las sales de carbonato a causa de una disminución del pH del medio?
Justifique la idoneidad de eliminar las incrustaciones de sales de carbonato con vinagre.
Ejercicio 1 · Opción B
1Opción B
2,5 puntosSèrie 3
El vinagre se obtiene mediante fermentación acética de vinos de baja graduación alcohólica, causada por bacterias aerobias de la familia Acetobacteraceae. El vino fermentado toma un gusto agrio cuando el etanol se convierte en ácido etanoico, también llamado ácido acético.
Una muestra de de vinagre presenta un grado de acidez de , expresado en gramos de ácido acético por litro de vinagre.
Calcule el pH del vinagre considerando que el único ácido presente en la muestra es el acético.
La determinación del grado de acidez del vinagre se lleva a cabo mediante una valoración ácido-base con hidróxido de sodio.
¿Cuántos mL de solución de hidróxido de sodio se necesitan para valorar de vinagre que tiene una concentración de ácido acético del en peso?
Ejercicio 2 · Opción A
2Opción A
2,5 puntosSèrie 1
La tabla periódica es una ordenación de los elementos químicos de número atómico creciente, de manera que se consiguen agrupaciones de elementos con propiedades atómicas, físicas y químicas parecidas, y variaciones continuas de estas propiedades.
Determine la configuración electrónica de los elementos flúor, neón y sodio.
Defina las propiedades periódicas: energía de ionización y afinidad electrónica.
Justifique el signo y el orden de magnitud de la energía de ionización para los tres elementos.
Justifique el orden de magnitud de la afinidad electrónica para los tres elementos.
Justifique cuál es el ion más estable que se formará de cada uno de los tres elementos anteriores.
Justifique cuál de los iones formados tiene un radio más pequeño.
Ejercicio 2 · Opción B
2Opción B
2,5 puntosSèrie 3
La policía ha encontrado una esterilla de acampada que podría resolver una investigación. Por eso hay que identificar su tipo de polímero entre el polietileno y el poliéster. Disponemos de un espectrofotómetro de infrarrojo para averiguar su identificación. Las estructuras de los dos polímeros son:
| Enlace | Tipo de compuesto | Intervalo de número de onda (cm-1) |
| C-H | alcanos (C-C-H) | 2970-2850 |
| alquenos (C=C-H) | 3095-3010 | |
| C-O | alcoholes, éteres, ácidos carboxílicos, ésteres | 1300-1050 |
| C=O | aldehídos, cetonas, ácidos carboxílicos, ésteres | 1760-1690 |
Describa los fundamentos de la técnica espectroscópica de infrarrojo. Justifique cuál es el polímero de acuerdo con su espectro de infrarrojo:
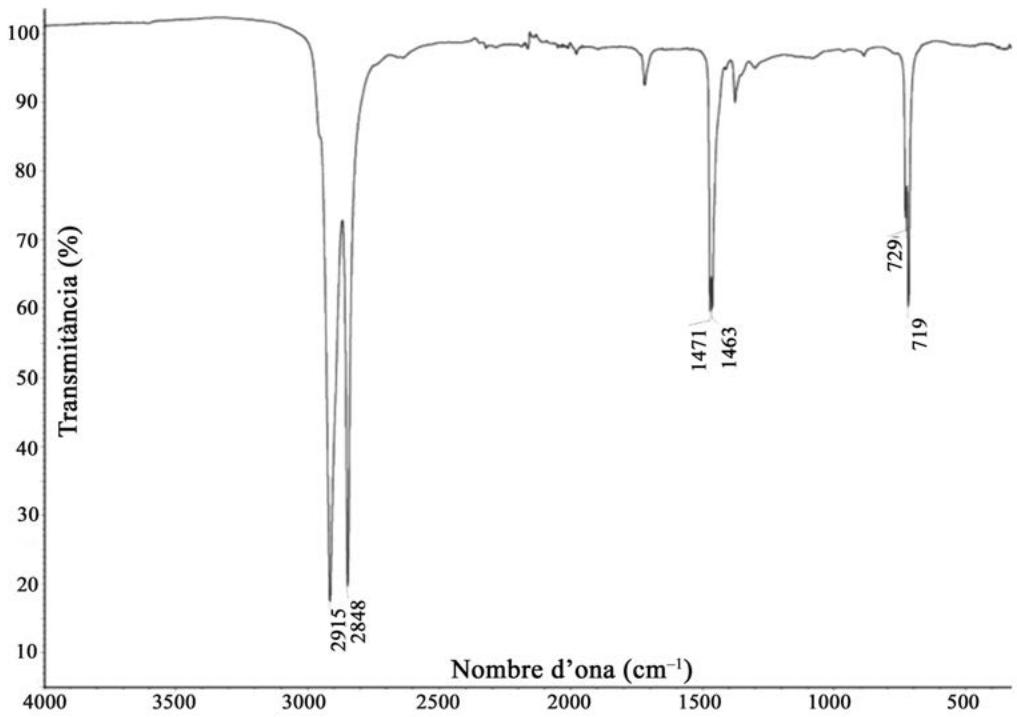
Identifique el pico de más energía del espectro anterior. Calcule la frecuencia, la longitud de onda y la energía correspondientes.
Ejercicio 3 · Opción A
3Opción A
2,5 puntosSèrie 1
El butano y el propano son dos combustibles gaseosos utilizados en la industria y el hogar. Las reacciones no ajustadas de combustión de estos gases son las siguientes:
Ajuste las reacciones.
Calcule la entalpía de combustión estándar del butano y del propano a presión constante.
Uno de los gases causantes del efecto invernadero es el . Justifique cuál de los dos combustibles genera más moles de por cantidad de calor liberada a presión constante.
Ejercicio 3 · Opción B
3Opción B
2,5 puntosSèrie 3
Actualmente se estudia la utilización del para almacenar energía solar. Cuando la energía solar incide sobre el situado dentro de un recipiente cerrado a alta temperatura, se disocia y produce y de acuerdo con la reacción ajustada siguiente:
Introducimos una cierta cantidad de en un recipiente de . Una vez alcanzado el equilibrio, hay de oxígeno. La de la reacción ajustada es a la temperatura del experimento. Calcule la concentración de todas las especies presentes en el equilibrio.
Explique en qué condiciones de presión y temperatura deberíamos trabajar para mantener el disociado y así almacenar la energía solar.
Ejercicio 4 · Opción A
4Opción A
2,5 puntosSèrie 1
Tenemos en el laboratorio dos soluciones de cada una. La primera es ácido clorhídrico con una concentración y la segunda es ácido acético de concentración desconocida. El pH medido de ambas soluciones es el mismo.
Determine:
— el pH de las dos soluciones ácidas;
— la concentración molar del ácido acético.
Se valoran separadamente de cada ácido con hidróxido de sodio .
Escriba las reacciones de neutralización.
Razone si el pH de los puntos de equivalencia de ambas valoraciones será ácido, básico o neutro.
Ejercicio 4 · Opción B
4Opción B
2,5 puntosSèrie 3
Una central térmica ha quemado el equivalente a de azufre y ha provocado un episodio de lluvia ácida. Se calcula que el del ácido sulfúrico producido ha caído dentro de un depósito cercano que contiene de agua. Las reacciones no igualadas que han ocurrido son:
Ajuste las reacciones.
Calcule la concentración de ácido sulfúrico en el depósito en unidades de y .
Haga los cálculos correspondientes y explique el procedimiento experimental que seguiría en el laboratorio para preparar de disolución de ácido sulfúrico de concentración a partir de ácido sulfúrico concentrado.
Indique el material de laboratorio necesario.
Ejercicio 5 · Opción A
5Opción A
2,5 puntosSèrie 1
La ecuación ajustada de formación del monóxido de nitrógeno a partir de sus elementos es la siguiente:
La constante de equilibrio de la reacción ajustada para formar de a una temperatura de es .
Indique la relación entre la y la . Calcule .
Determine las presiones parciales del nitrógeno y el oxígeno en el equilibrio, sabiendo que la presión del en el equilibrio es y que la presión del nitrógeno en el equilibrio es igual a la del oxígeno.
Si queremos favorecer la formación de monóxido, justifique qué variación de presión hay que aplicar a la reacción.
Ejercicio 5 · Opción B
5Opción B
2,5 puntosSèrie 3
Los hidruros de boro se han utilizado como combustibles de cohetes en la industria aeroespacial. Uno de estos hidruros, el , se inflama espontáneamente en el aire y da óxido de boro(III) y agua, de acuerdo con la reacción no ajustada siguiente:
Ajuste la reacción.
Calcule la cantidad de calor liberada cuando se quema del hidruro a la presión constante de .
La gasolina con un índice de octano («octanaje») alto está compuesta mayormente por octano líquido. Escriba la reacción ajustada de combustión del octano en la cual se obtiene dióxido de carbono gaseoso y agua líquida.
Calcule la energía obtenida en la combustión de de este hidrocarburo a volumen constante.
Ejercicio 6 · Opción A
6Opción A
2,5 puntosSèrie 1
En muchas series policiales hemos visto que los detectives utilizan un líquido que produce luminiscencia cuando se aplica sobre los lugares donde hay restos de sangre. Este líquido es una solución de luminol con peróxido de hidrógeno en medio básico. La reacción luminiscente se produce cuando el luminol es oxidado por el oxígeno que se forma al descomponerse el agua oxigenada:
Un requisito imprescindible es la presencia de un catalizador para la reacción anterior. En la detección de sangre, el catalizador es el hierro de la hemoglobina presente en los glóbulos rojos.
Para la reacción de descomposición del agua oxigenada:
— Dibuje el diagrama energético de la reacción catalizada y de la no catalizada.
— Compare la variación de entalpía de la reacción catalizada y de la no catalizada.
Teniendo en cuenta el modelo del estado de transición:
— ¿Qué es la energía de activación?
— Compare las energías de activación de la reacción catalizada y de la no catalizada.
— ¿Cómo se modifica la velocidad de reacción si aumentamos la temperatura?
Ejercicio 6 · Opción B
6Opción B
2,5 puntosSèrie 3
El metanotiol () es un gas incoloro con un olor similar a la col fermentada y es una de las principales sustancias responsables del mal aliento. Se produce de una manera natural con la descomposición bacteriana de las proteínas y, por tanto, se estudia como indicador de la degradación de alimentos.
Se sintetiza por reacción entre el metanol y el sulfuro de hidrógeno a , utilizando la alúmina y el wolframato de potasio como catalizadores:
Determine si la reacción será espontánea o no a esta temperatura.
Represente gráficamente el diagrama de energías de la reacción con catalizador, e indique la energía de activación y la entalpía de la reacción.
Explique cómo el catalizador modifica la velocidad de la reacción.
Indique también si el catalizador modifica la entalpía de la reacción. Justifique las respuestas.
Ejercicio 7 · Opción A
7Opción A
2,5 puntosSèrie 1
En el año 2019 el Premio Nobel de Química recompensó el desarrollo de las baterías de ion litio. Estas baterías se utilizan actualmente en dispositivos como teléfonos móviles, ordenadores portátiles y vehículos eléctricos.
Hay diversos modelos de baterías de ion litio; en uno de los modelos, el electrodo de litio es oxidado y el electrodo de azufre (S) es reducido a sulfuro () mediante un proceso complejo. La fuerza electromotriz estándar medida de una de estas baterías es .
Escriba las semirreacciones ajustadas que tienen lugar en cada electrodo y la reacción global. Indique la polaridad y el nombre de los electrodos.
Calcule el potencial estándar de reducción para la semirreacción del azufre en esta batería.
¿Cuántos gramos de litio se necesitan para construir una batería que funcione durante a una intensidad de ?
Ejercicio 7 · Opción B
7Opción B
2,5 puntosSèrie 3
Disponemos de una solución de sulfato de cobre(II) , una solución de sulfato de zinc , y una solución de , así como de láminas metálicas de y .
Justifique, a partir de los potenciales estándar de reducción de los pares redox, qué lámina debe ser el ánodo y cuál el cátodo para construir una pila.
Calcule la fuerza electromotriz de la pila.
Escriba la notación esquemática de la pila.
Escriba las reacciones que tienen lugar en el ánodo y en el cátodo y la reacción global de la pila. Explique el procedimiento experimental que deberíamos seguir para construir la pila.
Indique el material y los reactivos que necesitaremos.
