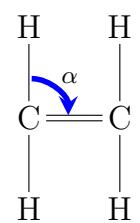
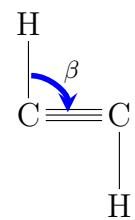
Se muestran, a continuación, las fórmulas estructurales semidesarrolladas del eteno y del etino. Justifique, utilizando los esquemas de hibridación de la teoría del enlace de valencia (TEV), los valores aproximados que toman los ángulos y .
Práctica rápida
Elige asignatura y tema. Puedes acotar por comunidad o año, o pedir otra tanda de ejercicios cuando quieras cambiar.
Temas
Para resolver