Copie la siguiente frase, completándola con dos de los términos que se proponen:
“Se trata de dos iones \_, que tienen el mismo número de \_”
“isotópicos”, “isotónicos”, “isoelectrónicos”, “protones”, “neutrones”, “electrones”
QuímicaMurciaPAU 2025Extraordinaria
Química · Murcia 2025
10 ejercicios90 min de duración
Datos generales del examen
- Masas atómicas ():
Ejercicio 1 · Opción A
1Opción A
2 puntosBLOQUE 1. ESTRUCTURA ATÓMICA Y ENLACE QUÍMICO
Elegir una cuestión, 1A o 1B.
Considere los iones y y conteste a las siguientes cuestiones:
Escriba la configuración electrónica de ambos iones e indique con qué gas noble coincide.
Indique qué catión monopositivo posee la misma configuración electrónica que dichos iones.
Razone brevemente cuál de los dos iones, y , tendrá un radio menor.
Considere el proceso de formación de los aniones y a partir de los átomos neutros, siendo la primera afinidad electrónica y la segunda afinidad electrónica de cada elemento:
Explique razonadamente a cuál de las tres afinidades electrónicas, , y corresponderá cada uno de los tres siguientes valores:
Ejercicio 1 · Opción B
1Opción B
2 puntosBLOQUE 1. ESTRUCTURA ATÓMICA Y ENLACE QUÍMICO
Elegir una cuestión, 1A o 1B.
El es un líquido incoloro que se utiliza en la industria como disolvente y en la elaboración de refrigerantes, resinas y plásticos. Dejó de utilizarse como anestésico en cirugías por sus efectos adversos en el organismo. El se ha usado como disolvente, desengrasante y refrigerante, entre otras aplicaciones, pero ha caído prácticamente en desuso por su muy alta toxicidad.
Nombre ambas sustancias.
Represente sus estructuras de Lewis y, en base a ellas, explique brevemente cómo será la geometría y polaridad de estas moléculas.
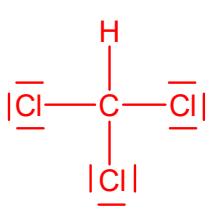
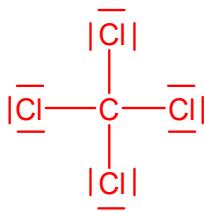
Explique si una mezcla equimolar de y será conductora de la electricidad.
Considere la siguiente tabla:
Puede verse que los puntos de ebullición de los tres compuestos son bastante similares. Sin embargo, las interacciones intermoleculares son diferentes en cada uno de ellos. Explique brevemente qué interacciones intermoleculares predominan en cada uno de ellos, y por qué el punto de ebullición del es el mayor de los tres.
| Peso molecular (g·mol-1) | Punto de ebullición | |
| CCl4 | 154 | 76,7 °C |
| CHCl3 | 119,5 | 61,2 °C |
| CH3OH | 32 | 64,7 °C |
Ejercicio 2 · Opción A
2Opción A
2 puntosBLOQUE 2. REACCIONES REDOX
Elegir una cuestión, 2A o 2B.
La corrosión es un proceso de degradación de los metales debido a reacciones con su entorno. Se trata de un problema de gran magnitud que causa graves daños a infraestructuras y equipos, con un elevado impacto económico (un 3,5% del PIB mundial). Uno de los procesos implicados en la corrosión es la oxidación. El Al es un metal muy reductor (), por lo que no debería ser adecuado como material de construcción. En cambio, es ampliamente utilizado, y esto es debido a que se pasiva, recubriéndose de una fina capa de óxido que actúa como barrera protectora frente a la corrosión de todo el material.
Explique brevemente qué significa que el Al es muy reductor.
Un método industrial para pasivar el Al es mediante su reacción con en medio ácido, generando iones y la capa protectora de . La reacción, en forma iónica y sin ajustar, es:
Ajuste la reacción, en forma iónica, mediante el método del ion-electrón, indicando cuál es la semirreacción de reducción y cuál la de oxidación.
Nombre los compuestos y .
Explique brevemente cómo variará el pH durante el transcurso de la reacción.
Ejercicio 2 · Opción B
2Opción B
2 puntosBLOQUE 2. REACCIONES REDOX
Elegir una cuestión, 2A o 2B.
Una forma de evitar la corrosión en equipamientos, como cascos de buques, oleoductos o tanques, es emplear “ánodos de sacrificio”, también llamados ánodos galvánicos. Como su nombre indica, se trata de piezas de metal que se oxidan más fácilmente que el metal a proteger, evitando que este se corrompa.
Entre el Fe y el Mg, explique brevemente cuál de ellos sería el componente del ánodo de sacrificio, protegiendo al otro de la oxidación.
El ánodo de sacrificio debe estar en contacto físico con el metal a proteger de forma que, si dicho metal es oxidado por el entorno, el ánodo de sacrificio actuará, reduciéndolo de nuevo.
Escriba la reacción redox ajustada que se produciría entre el y el Mg. Para ello escriba primero las semirreacciones de oxidación y reducción, indicando cuál es cada una.
Indique cuántos electrones se intercambian en dicha reacción.
Calcule el potencial de dicha reacción (fuerza electromotriz) y la variación de energía libre, indicando si se trata de una reacción espontánea o no.
Razone brevemente si será necesario reemplazar los ánodos de sacrificio cada cierto tiempo.
Ejercicio 3 · Opción A
3Opción A
2 puntosBLOQUE 3. ÁCIDO-BASE
Elegir una cuestión, 3A o 3B.
Muchos ácidos carboxílicos se emplean como aditivos alimentarios. Por ejemplo, el tiene efecto antimicrobiano y es eficaz como conservante si su pH es inferior a 5. Se dispone de una disolución acuosa de este ácido, disociada en un . Responda a las siguientes cuestiones:
Nombre el .
Calcule el pH de la disolución y, en función del valor obtenido, determine si será efectiva como conservante.
Calcule el valor de para el .
Compruebe si el valor de obtenido es compatible con un valor de para el .
Explique cualitativamente cómo variará el pH de la disolución de si se adiciona una cierta cantidad de benzoato de sodio.
Ejercicio 3 · Opción B
3Opción B
2 puntosBLOQUE 3. ÁCIDO-BASE
Elegir una cuestión, 3A o 3B.
El se utiliza en extintores de incendios, pues se transforma fácilmente en que, a su vez, se descompone liberando una densa nube de , que desplaza al en las proximidades del fuego, sofocándolo. Esta reacción se puede recrear en un experimento casero, mezclando en una botella de plástico (con un orificio de salida), y vinagre (disolución acuosa de ):
Nombre los compuestos y e indique cuál de ellos está actuando como un ácido y cuál como una base, en la primera reacción.
Según la etiqueta de un vinagre casero comercial, su concentración es de (grados acéticos), que equivale a de en de agua. ¿Qué volumen de este vinagre será necesario para reaccionar completamente con de ?
Si un extintor comercial contiene de y se usa completamente para extinguir un fuego, calcule el volumen de que se generará, a presión atmosférica, suponiendo que la temperatura que se alcanza en la llama es de .
En la reacción del enunciado se forma . Sabiendo que el es un ácido débil, explique brevemente si una disolución de en agua será ácida, básica o neutra. (No es necesario realizar cálculos numéricos, ni escribir reacciones químicas).
Ejercicio 4 · Opción A
4Opción A
2 puntosBLOQUE 4. TERMOQUÍMICA, EQUILIBRIO Y CINÉTICA
Elegir una cuestión, 4A o 4B.
En tres experimentos distintos, realizados a la misma temperatura pero con distintas concentraciones iniciales de los reactivos, se obtuvieron las siguientes velocidades iniciales para la reacción:
Estime el orden de la reacción respecto a cada uno de los reactivos, explicando su respuesta, y escriba la ecuación de velocidad:
| Exp. | [NO]initial (mol·L-1) | [H2]initial (mol·L-1) | velocidad inicial de reacción, M·s-1 |
| 1 | 0,10 | 0,10 | 1,23·10-3 |
| 2 | 0,10 | 0,20 | 2,46·10-3 |
| 3 | 0,20 | 0,10 | 4,92·10-3 |
Se realizó un cuarto experimento, en el que se olvidaron de anotar el valor de la . Deduzca cuál será ese valor, si el resto de datos del experimento son los siguientes:
| Exp. | [NO]inicial (mol·L-1) | [H2]inicial (mol·L-1) | velocidad inicial de reacción, M·s-1 |
| 4 | 0,10 | ¿x? | 3,69·10-3 |
Si en un instante dado el se está formando a una velocidad de , ¿a qué velocidad se estará consumiendo, en ese mismo instante, el NO?
Explique brevemente de qué tipo de reacción se trata (ácido-base, precipitación, redox, desplazamiento, oxidación…).
Observando la ecuación química, explique si la entropía aumenta o disminuye.
Ejercicio 4 · Opción B
4Opción B
2 puntosBLOQUE 4. TERMOQUÍMICA, EQUILIBRIO Y CINÉTICA
Elegir una cuestión, 4A o 4B.
Una bombona de butano estándar contiene de gas butano licuado, a alta presión. Cuando se abre la válvula de la bombona se permite la evaporación de parte del butano, que se mezcla con el oxígeno del aire y se quema, liberando energía en forma de calor.
Complete y ajuste la reacción de combustión un mol de butano:
Calcule el volumen que ocuparía todo el butano de la bombona, a y .
Si para la combustión de un mol de butano y :
Calcule la energía obtenida de la combustión total de una bombona de butano, expresando el resultado con dos cifras significativas.
Calcule el valor de a , expresando el resultado también con dos cifras significativas, y explique si la reacción será espontánea en condiciones estándar a dicha temperatura.
Ejercicio 5 · Opción A
5Opción A
2 puntosBLOQUE 5. QUÍMICA ORGÁNICA
Elegir una cuestión, 5A o 5B.
Considere la siguiente reacción:
Indique qué tipo de reacción orgánica es.
Nombre los compuestos A, B1 y B2.
Los compuestos B1 y B2 son isómeros entre sí. Indique el tipo y subtipo de isomería que presentan. Indique también cuál de ellos se formará mayoritariamente.
Explique brevemente si cada uno de los compuestos A, B1 y B2, puede presentar isomería espacial, y de qué tipo sería.
Si la reacción de A con no tiene lugar en caliente, se forma un producto distinto, C, junto con y sin formación de . Escriba la fórmula de C, e indique el tipo de reacción orgánica de que se trata.
Ejercicio 5 · Opción B
5Opción B
2 puntosBLOQUE 5. QUÍMICA ORGÁNICA
Elegir una cuestión, 5A o 5B.
Considere las siguientes parejas de compuestos:
Para la pareja A: escriba su fórmula semidesarrollada, nómbrela y explique si posee algún carbono asimétrico.
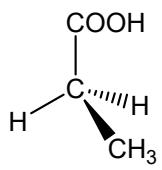
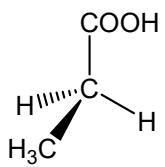
Para la pareja B: escriba su fórmula molecular, nombre el compuesto B1 y explique si los dos compuestos, B1 y B2, son isómeros y, en caso afirmativo, de qué tipo y subtipo.
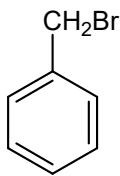
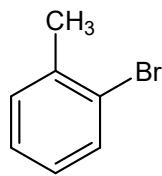
Se lleva a cabo la reacción de tolueno con en presencia de , obteniéndose una mezcla de tres productos que son isómeros de posición. El de la mezcla corresponde al compuesto B2 del enunciado, el a un isómero minoritario, B3, y el al isómero mayoritario, B4, que es el p-bromotolueno.
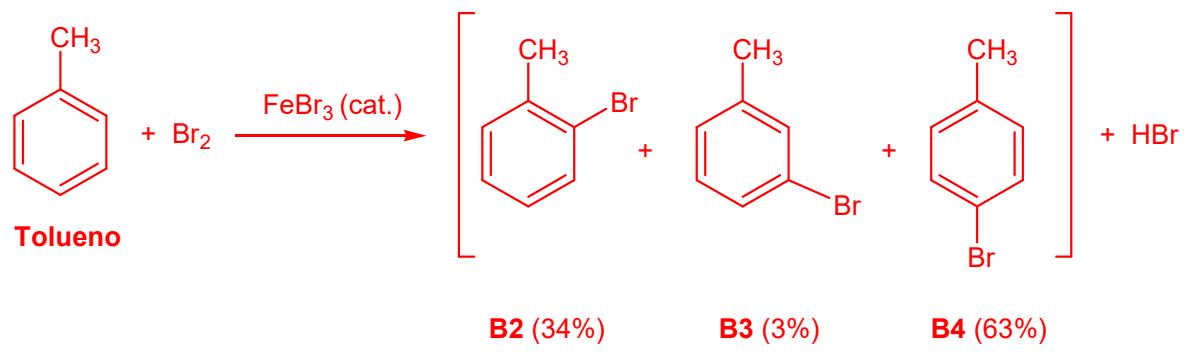
Copie la reacción dibujando las fórmulas del tolueno y de los tres isómeros B2, B3 y B4, y nombre los productos B2 y B3.
Indique qué tipo de reacción orgánica es.
