Escriba las dos reacciones de combustión. Calcule la entalpía estándar de reacción de cada combustible a . Si le pidieran consejo para elegir uno de los dos combustibles para hacer señales desde un barco, considerando que la bodega del barco está casi al límite del peso permitido, ¿cuál de los dos aconsejaría? Justifique la respuesta.
QuímicaCataluñaPAU 2023Ordinaria
Química · Cataluña 2023
14 ejercicios
Ejercicio 1 · Serie 1
1Serie 1
2,5 puntosSerie 1
La hidrazina () y la dimetilhidrazina () son combustibles líquidos. La hidrazina reacciona con el oxígeno y se obtiene y . La dimetilhidrazina reacciona con el oxígeno y se obtiene , y .
| Sustancia | ||||
|---|---|---|---|---|
| () | 50,6 | 42,0 | -241,8 | -393,5 |
Represente el diagrama entálpico del proceso de combustión de la hidrazina. En la etiqueta de un envase que contiene hidrazina se observan los dos pictogramas siguientes. Explique qué significan estos pictogramas y de qué peligros nos alertan.


Ejercicio 1 · Serie 5
1Serie 5
2,5 puntosSerie 5
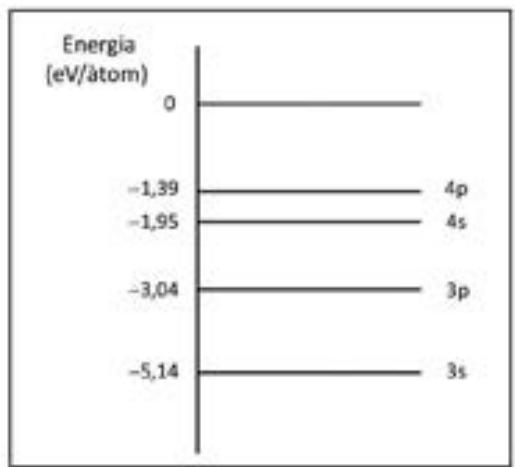
El diagrama de la figura adjunta representa la energía de algunos orbitales que pueden ser ocupados por el electrón más externo del átomo de sodio.
| Color de la radiación | violeta | azul | verde | amarillo | naranja | rojo |
|---|---|---|---|---|---|---|
| Longitud de onda (nm) | 380-450 | 450-495 | 495-570 | 570-590 | 590-620 | 620-750 |
Defina el término orbital atómico según el modelo ondulatorio del átomo, y escriba la configuración electrónica del átomo de sodio en estado fundamental. Explique qué es la energía de ionización de un átomo y calcule su valor para el átomo de sodio, expresado en .
En el espectro de emisión del sodio se observa una línea intensa que corresponde a la transición electrónica . ¿De qué color es esta radiación?
Ejercicio 2 · Serie 1
2Serie 1
2,5 puntosSerie 1
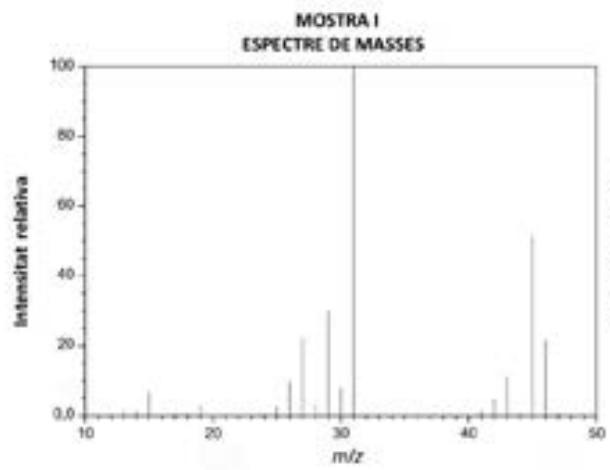
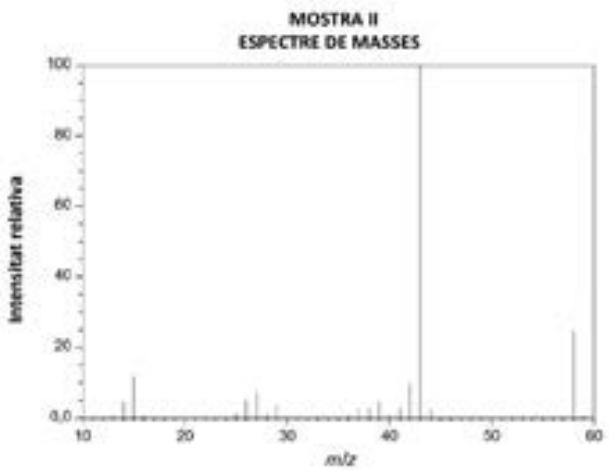
En una empresa química que produce disolventes tienen un problema de identificación de dos lotes elaborados, uno de etanol y otro de acetona, también llamada propanona. Para poder identificar qué disolvente hay en cada lote, realizan un espectro de masas de una muestra de cada uno de los lotes.
Formule el etanol y la acetona. Indique cuál es el pico base y el pico del ion molecular de los espectros de cada muestra. ¿Qué información nos dan estos picos? ¿Qué espectro corresponde a cada disolvente? Justifique las respuestas.
El pico característico para identificar una cetona en un espectro de absorción infrarrojo (IR) corresponde a un número de onda de . Calcule la longitud de onda, la frecuencia y la energía correspondientes a este pico.
Ejercicio 2 · Serie 5
2Serie 5
2,5 puntosSerie 5
Para montar una pila, en condiciones estándar y a , disponemos de una placa metálica de cobre y otra de aluminio, una botella que contiene una solución de sulfato de cobre(II) y otra botella que contiene una solución de cloruro de aluminio.
Justifique qué electrodo actuará como cátodo y cuál como ánodo en esta pila. Escriba las semirreacciones que tendrán lugar en cada electrodo, la reacción iónica global y la notación de la pila. Calcule su fuerza electromotriz estándar (FEM).
Explique cómo montaría esta pila en el laboratorio, e indique el material y las otras sustancias químicas que necesitaría. Haga un dibujo del montaje experimental.
Ejercicio 3 · Serie 1
3Serie 1
2,5 puntosSerie 1
El cloruro de sulfurilo () es un líquido a temperatura ambiente de olor punzante que a menudo se utiliza como fuente de cloro gaseoso, ya que por ser un líquido es más fácil de almacenar y manipular. Es muy empleado en la síntesis de compuestos orgánicos para transformar enlaces en enlaces . También se ha utilizado en el tratamiento de la ropa de lana para que no encoja. El cloruro de sulfurilo se obtiene industrialmente por reacción entre el cloro y el dióxido de azufre, usando carbón activo como catalizador. Se ha realizado la reacción de obtención de en un recipiente cerrado de a :
Cuando la reacción ha alcanzado el equilibrio, se ha comprobado que el recipiente contenía de , de y de . Determine el valor de la constante de equilibrio en concentraciones (). Si, después de alcanzar el equilibrio, se añaden de a la mezcla de reacción, ¿cuál es la nueva concentración de cloruro de sulfurilo en el equilibrio?
Razone qué efecto tendría sobre el rendimiento de la reacción un aumento de la temperatura del recipiente, un aumento del volumen del recipiente y la eliminación del catalizador. Razone también qué efecto tendrían sobre el valor de las tres acciones mencionadas anteriormente.
Ejercicio 3 · Serie 5
3Serie 5
2,5 puntosSerie 5
En las bodegas donde se elabora vino, y durante el tiempo que dura el proceso de fermentación del mosto, se oye un susurro constante que rompe el silencio, aquello que en el mundo de la enología se conoce con la expresión «el vino hierve». El azúcar (glucosa) se convierte en etanol y, al mismo tiempo, se produce dióxido de carbono gaseoso:
glucosa etanol
Sabemos que las entalpías estándar de combustión de la glucosa y del etanol son, respectivamente, y . Calcule el calor que se desprende, a presión constante, cuando se forma un mol de etanol por fermentación de la glucosa.
Nota: Las entalpías estándar de combustión están expresadas por mol de sustancia que se quema.
En las tablas termodinámicas podemos encontrar la entalpía estándar de formación de un compuesto. Escriba la reacción química correspondiente a la entalpía estándar de formación del etanol gaseoso, y estime su valor a partir de los datos de energía de enlace siguientes:
| Enlace | C-C | C-O | C-H | H-H | O-H | O=O |
|---|---|---|---|---|---|---|
| Energía de enlace () | 347 | 360 | 414 | 436 | 464 | 498 |
Ejercicio 4 · Serie 1
4Serie 1
2,5 puntosSerie 1
El ácido hipocloroso () se considera uno de los desinfectantes más potentes y se utiliza en centros sanitarios con la voluntad de extremar las medidas de desinfección de sus instalaciones a raíz de la covid-19. A menudo este ácido débil se utiliza como desinfectante en soluciones de concentración .
Calcule la constante de acidez del ácido hipocloroso, sabiendo que una solución acuosa de este ácido tiene un pH de a . Otro ácido, el ácido cloroso (), tiene una constante de acidez de . ¿Qué pH tendrá una solución de concentración de este segundo ácido?
Al valorar de una solución de desinfectante, de concentración de ácido hipocloroso desconocida, con una solución acuosa de hidróxido de sodio () , necesitamos de esta base para llegar al punto final. Escriba la reacción de valoración. ¿Cuál es la concentración de ácido hipocloroso en el desinfectante? ¿Esta concentración es mayor o menor que la concentración habitual de los desinfectantes empleados más frecuentemente? Diga si el pH en el punto de equivalencia será ácido, neutro o básico, y justifique la respuesta.
Ejercicio 4 · Serie 5
4Serie 5
2,5 puntosSerie 5
El yoduro de hidrógeno es un gas incoloro, fácilmente soluble en agua, que se utiliza en química como agente reductor. Lo podemos sintetizar a partir de yodo e hidrógeno, en fase gaseosa, según la reacción siguiente:
En un reactor de mezclamos de , de y de ; lo calentamos a de temperatura, y se inicia la reacción. Dos horas más tarde, observamos que el reactor contiene de .
Calcule las concentraciones de las tres sustancias cuando han transcurrido dos horas desde el inicio de la reacción, y el valor del cociente de reacción () en este momento. Diga si el contenido del reactor está en equilibrio o no lo está, y justifique la respuesta.
Suponga que, después de cinco horas, la cantidad de se estabiliza, de manera que ni aumenta ni disminuye si dejamos transcurrir más tiempo. Justifique qué efecto tendría sobre la cantidad de moles de si, en este momento, disminuimos el volumen del reactor, eliminamos una parte del hidrógeno gaseoso del reactor, introducimos un catalizador en el reactor y aumentamos la temperatura del reactor.
Ejercicio 5 · Serie 1
5Serie 1
2,5 puntosSerie 1
El acetaldehído () se descompone en metano y monóxido de carbono según la reacción siguiente:
Esta reacción tiene una energía de activación de sin utilizar ningún catalizador y una energía de activación de utilizando yodo como catalizador.
| Sustancia | ||
|---|---|---|
| () | -75 | -111 |
Justifique si se trata de una reacción endotérmica o exotérmica. Calcule el valor de la entalpía estándar de formación del acetaldehído a . Dibuje en un mismo gráfico la energía de la reacción en función de la coordenada de reacción de la reacción catalizada y no catalizada, indicando la posición de los estados de transición, las energías de activación y la entalpía de reacción.
Determine las energías de activación de la reacción de síntesis del acetaldehído a partir de metano y monóxido de carbono del proceso catalizado y no catalizado. ¿Qué es un catalizador? Razone, a partir del modelo cinético del estado de transición, cómo afecta un catalizador a la velocidad de la reacción.
Ejercicio 5 · Serie 5
5Serie 5
2,5 puntosSerie 5
A raíz de la pandemia provocada por el coronavirus SARS-CoV-2, a mediados de marzo de 2020 la Agencia Catalana de Seguridad Alimentaria publicó en su web un conjunto de recomendaciones de limpieza y desinfección de instalaciones de empresas alimentarias para la prevención de este virus. La Agencia recomendó el uso, como desinfectante, de una solución de hipoclorito de sodio () al en masa, después de la limpieza con un detergente neutro.
Escriba la reacción del ion hipoclorito en agua. Calcule el pH, a , de la solución desinfectante que recomendaba la Agencia. Suponga que la densidad de la solución es .
Para seguir uno de los métodos de fabricación de hipoclorito de sodio, necesitamos cloro gaseoso (). Podemos obtener este cloro principalmente mediante la electrólisis de cloruro de sodio, utilizando un cátodo de mercurio y un ánodo de titanio:
Efectuamos la electrólisis de de una solución de empleando una corriente constante de . ¿Cuál será la concentración de cloro que habrá en la celda electrolítica después de minutos?
Ejercicio 6 · Serie 1
6Serie 1
2,5 puntosSerie 1
El sulfato de bario () es un compuesto poco soluble en agua que se utiliza como contraste radiológico en análisis de rayos X del esófago, el estómago y los intestinos. Generalmente, hay que beber una suspensión de sulfato de bario una o dos veces antes del análisis radiológico.
Calcule la solubilidad molar del sulfato de bario en agua. Calcule qué cantidad de ion bario (), en mg, se ingiere si se toman de una solución saturada de sulfato de bario antes de un análisis radiológico.
Algunos estudios indican que aproximadamente el de la población es alérgica al ion bario. En caso de que un paciente sea alérgico al ion bario, razone si añadir una cierta cantidad de sulfato de sodio () a la suspensión de sulfato de bario que debe tomar sería bueno para disminuir los efectos de la alergia. A las personas alérgicas al ion bario, ¿qué suspensión les provocará más alergia: una de sulfato de bario o una de carbonato de bario ()? Justifique la respuesta.
Ejercicio 6 · Serie 5
6Serie 5
2,5 puntosSerie 5
En la superficie terrestre, el ozono () es uno de los indicadores de la contaminación del aire. Diversos estudios indican que, cuando el ozono se encuentra en estado estacionario, es decir, cuando la velocidad de la reacción de producción y de destrucción del ozono es la misma, su concentración es . Suponga que el único proceso de destrucción del ozono es la formación de oxígeno molecular, según la reacción química siguiente:
Escriba la ecuación de velocidad de la reacción de destrucción del ozono, si sabemos que sigue una cinética de segundo orden. Calcule la constante de velocidad de esta reacción si estimamos que la producción del ozono debida a todas las fuentes es , y que el ozono se encuentra en estado estacionario. Explique, a partir de un modelo cinético, cómo afecta la temperatura a la velocidad de reacción.
Calcule la energía de Gibbs estándar de la reacción de destrucción del ozono a y justifique que es espontánea. Si sabemos que la espontaneidad de esta reacción no depende de la temperatura, razone si la reacción es endotérmica o exotérmica.
Ejercicio 7 · Serie 1
7Serie 1
2,5 puntosSerie 1
El recubrimiento electrolítico con cromo se utiliza para proteger superficies metálicas de la corrosión, así como para mejorar su aspecto y sus prestaciones.
Se quiere cromar un objeto de acero rectangular que tiene una superficie de con una capa de cromo de de grosor. Para hacerlo, se coloca este objeto como cátodo en una cubeta de electrólisis que contiene iones en solución. Escriba la reacción de electrodeposición del cromo. Si la corriente es de , ¿cuántas horas debe durar la electrólisis?
Los ánodos de sacrificio también se utilizan como sistema de protección anticorrosivo. Estos recubrimientos se oxidan antes que el metal que protegen. Justifique cuáles de los metales de la tabla siguiente podrían utilizarse como ánodos de sacrificio para proteger una superficie que contiene hierro. Defina oxidante y reductor. En la vida cotidiana, ¿cuáles son los principales agentes causantes de la corrosión de los metales?
| 0,52 V | -0,28 V | -0,44 V | -0,76 V | -1,66 V | -2,37 V |
Ejercicio 7 · Serie 5
7Serie 5
2,5 puntosSerie 5
La litiasis urinaria consiste en la presencia de cálculos en el riñón o en las vías urinarias debidos a concentraciones altas de ciertas sustancias que deberíamos eliminar por la orina. En la litiasis cálcica, que es la más frecuente, estos cálculos se forman a causa de un aumento de la concentración de calcio en la orina, que provoca la precipitación de diversas sales, como el fosfato de calcio, .
¿Podemos disolver, a , un cálculo de de fosfato de calcio en de agua? Razónelo cuantitativamente.
En cuatro tubos de ensayo ponemos un poco de fosfato de calcio sólido en contacto con de solución acuosa saturada de esta sal. Añadimos a cada uno de los tubos unos mililitros de las soluciones que se muestran en la tabla siguiente. Explique, razonada y cualitativamente, qué observaremos en cada tubo.
Nota: EDTA (ácido etilendiaminotetraacético): ligando orgánico que forma complejos solubles con muchos iones metálicos (incluidos los alcalinotérreos).
| Tubo | Tubo 1 | Tubo 2 | Tubo 3 | Tubo 4 |
|---|---|---|---|---|
| Sustancia añadida | EDTA(aq) |
